- Анатомические особенности щитовидной железы
- Заболеваемость и смертность. Факторы, способствующие развитию рака щитовидной железы. Вопросы классификации
- Клинико-морфологическая характеристика опухолей
- Особенности клинического течения опухолей
- Своеобразно протекающие формы рака щитовидной железы
- Комплексная диагностика опухолей
- Лечебная тактика при раке щитовидной железы
- Хирургическое лечение
- Дополнительные методы лечения
- Результаты лечения
C73 Злокачественное новообразование щитовидной железы, МКБ-10
Отредактировано: 02.04.2024
Разбирая вопросы диагностики и лечения опухолей щитовидной железы, невозможно не коснуться анатомического строения этого органа, особенно принимая во внимание тот факт, что основным методом лечения до настоящего времени остается хирургический.
Анатомические особенности щитовидной железы
Щитовидная железа является наиболее крупной из всех органов внутренней секреции у взрослых. Это достаточно плоское образование красного цвета, имеющее массу от 20 до 60 г. Она состоит из двух долей и перешейка, который в 2—10% случаев может отсутствовать. Доли щитовидной железы располагаются по обеим сторонам 1—5 колец трахеи, чуть ниже щитовидного хряща (рис. 1).
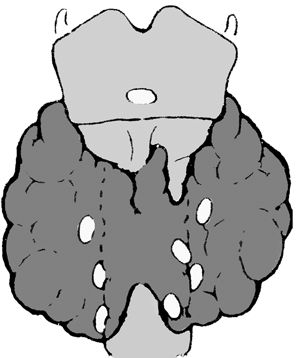
Рисунок 1. Строение щитовидной железы
В 30% случаев в области перешейка, на передней поверхности шеи кверху отходит пирамидальный отросток, который может распространяться до подъязычной кости. Правая доля щитовидной железы, как правило, больше левой. Сзади доли щитовидной железы соприкасаются со стенками глотки и пищевода (преимущественно слева).
Шейная часть пищевода, начавшись со средней линии позади трахеи, на уровне CVI, т.е. соответственно нижнему краю перстневидного хряща, уклоняется влево. Это очень важно знать, т.к. при мобилизации левой доли щитовидной железы, особенно пораженной опухолью, возможно повреждение пищевода.
Перешеек задней поверхностью прилежит к 2–3–4 кольцам трахеи, но иногда распространяется до 6 кольца. Это необходимо помнить при трахеотомии, особенно нижней, т.к. при мобилизации трахеи могут возникнуть трудности.
Щитовидная железа человека начинает развиваться на 2–4-й неделе эмбрионального периода. Она возникает из медиального зачатка, развивающегося из утолщения ротоглоточного эпителия в месте, впоследствии соответствующем слепому отверстию корня языка. Ее происхождение берет начало из парных латеральных зачатков, появляющихся в области четвертого жаберного кармана. С ростом эпителия срединный зачаток внедряется вглубь подлежащих тканей в виде щитовидно-язычного протока. Последний в процессе развития облитерируется и на 8 нед эмбрионального периода превращается в шнур эпителиальных клеток, тянущийся от слепого отверстия языка до трахеи. На 4—5 нед развития подъязычная кость делит щитовидно—язычный проток на язычный, идущий к корню языка, и щитовидный. Эти детали необходимо знать, т.к. в некоторых случаях облитерации щитовидно—язычного протока не происходит, и в этих случаях образуются срединные кисты и свищи шеи. Чаще они локализуются в щитовидной части щитовидно—язычного протока, крайне редко — в язычном отделе. При этом во втором случае надо делать надподъязычную фаринготомию с резекцией корня языка. В первом же, при удалении кисты необходимо обязательно резецировать тело подъязычной кости. В противном случае высока вероятность рецидива срединной кисты или свища шеи.
Кроме возможности возникновения срединных кист и свищей шеи, значительно реже встречаются в этой области, а особенно в корне языка, эктопированные зобы. Это обусловливается тем, что в процессе эмбриогенеза по пути отхождения щитовидно—язычного протока происходит отшнуровка отдельных клеток. Исследования на 117 трупах, проведенные Р.И. Венгловским еще в 1909 г., показали: у 26 — в корне языка обнаруживались частицы ткани щитовидной железы, а у 45 — элементы щитовидной железы имелись в надкостнице подъязычной кости. В некоторых случаях зачаток щитовидной железы может весь не спуститься из области слепого отверстия языка, и железа на обычном месте отсутствует. Это важно знать при планировании операций по поводу так называемого зоба корня языка, т.к. полное его удаление может привести к микседеме.
Щитовидная железа имеет наружную и внутреннюю капсулы. Наружная капсула окутывает железу вместе с гортанью, внутренняя — плотно срастается с ее паренхимой, покрывает собственно железу. Между обеими капсулами имеется щелевидное пространство, в котором проходят многочисленные кровеносные сосуды.
На задней поверхности боковых долей между собственной и фасциальной капсулами в жировой клетчатке располагаются паращитовидные железы, количество которых колеблется от 2—3 до 5—6, а иногда и до 12. Они находятся кнаружи от возвратного нерва, иногда прилегая к последнему. Располагаются паращитовидные железы соответственно верхнему полюсу щитовидной железы, у входа возвратного нерва в гортань, и у нижнего полюса. Их легко спутать с жировой клетчаткой, лимфатическими узлами, а иногда — с паратрахеальными метастазами небольших размеров. При операции на щитовидной железе, особенно в объеме тиреоидэктомии, надо стараться максимально сохранить паращитовидные железы, т. к. при их удалении могут развиться явления тетании. Последняя может появиться и при сохранении паращитовидных желез в результате перевязки и пересечения проходящих в капсуле щитовидной железы артериальных веточек, питающих железу.
Кровоснабжение щитовидной железы осуществляется двумя верхними, двумя нижними и одной непарной щитовидной артериями. Последняя, как правило, отходит от плечеголовного ствола, реже — от подключичной артерии. Нижняя щитовидная артерия располагается рядом с возвратным нервом, который в 43% случаев проходит между ее ветвями. Верхняя щитовидная артерия отходит от наружной сонной артерии, чуть выше развилки общей сонной, а иногда и на ее уровне. Артерия входит в верхний полюс щитовидной железы, как правило, одним стволом. Однако в некоторых случаях она делится на несколько веточек. Это надо знать при мобилизации верхнего полюса щитовидной железы, когда лигируется верхний сосудисто—нервный пучок.
Возвратный нерв, обычно единичный, в 60% случаев входит в гортань одним стволом, в 40% случаев — делится на уровне нижнего полюса щитовидной железы на две, а иногда и большее количество ветвей. Дистальная часть возвратного нерва образует нижний гортанный нерв.
Венозная система щитовидной железы развита больше, чем артериальная и также богата анастомозами. Причем ряд авторов описывают наличие лимфовенозных анастомозов.
Лимфатические сосуды щитовидной железы собирают лимфу в предгортанные (дельфиниев узел), претрахеальные, паратрахеальные, глубокие яремные лимфатические узлы, а также лимфатические узлы переднего средостения (рис. 2).
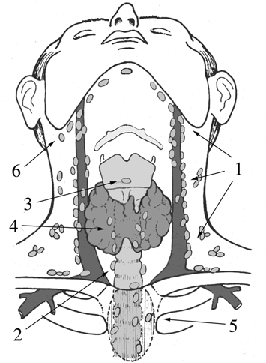
Рисунок 2. Схема лимфооттока из щитовидной железы:
1 — верхние, средние и нижние глубокие яремные лимфатические узлы; 2 — паратрахеальные лимфатические узлы; 3 — предгортанный (дельфиниев) узел; 4 — претрахеальные лимфатические узлы; 5 — лимфатические узлы верхнего средостения; 6 — лимфатические узлы акцессорной зоны
Именно в этих группах лимфатических узлов могут реализоваться регионарные метастазы при раке щитовидной железы.
Симпатическая иннервация щитовидной железы осуществляется нервами, идущими от шейных симпатических стволов. Парасимпатическая иннервация обеспечивается ветвями блуждающего нерва — верхним гортанным и возвратным.
Функция щитовидной железы тесно связана с обменом йода в организме, при этом йод специфически концентрируется в щитовидной железе. Тиреоидные гормоны выполняют, главным образом, функцию регуляторов процесса окисления в клетках. Главная функция щитовидной железы — секреция специфического гормона. Основной гормон щитовидной железы — тироксин — открыт еще в начале прошлого века. В середине прошлого века в щитовидной железе обнаружен трийодтиронин — более сильнодействующий гормон по сравнению с тироксином. Гормоны щитовидной железы в просвете фолликулов связаны с тиреоглобулином. Общее действие этих гормонов сводится к стимуляции всех видов обмена вещества, но механизмы этого воздействия еще окончательно не выявлены.
Заболеваемость и смертность. Факторы, способствующие развитию рака щитовидной железы. Вопросы классификации
Частота узловых образований щитовидной железы по оценкам различных исследователей середины ХХ в. составляла от 3 до 7%. Однако внедрение в клиническую практику УЗКТ показало, что узловые образования в щитовидной железе выявляются значительно чаще и составляют около 50%, особенно у женщин старше 50 лет. Частота реализации рака в узловых образованиях, по данным различных авторов, варьирует, но в среднем составляет 25—30%.
Из 1121 пациента, лечившегося в нашей клинике с 1981 по 2000 г., диагноз рака был установлен у 66,1% пациентов, узловой зоб — у 16%, аденома — у 13%, у 43% узловые образования сочетались с аутоиммунным тиреоидитом. Эти цифры, однако, не отражают истинную частоту появления того или иного образования при узловом поражении щитовидной железы. Они, скорее, свидетельствуют о контингенте больных с опухолевыми поражениями щитовидной железы, лечившихся в специализированной онкологической клинике. С этой точки зрения значительно интереснее опыт эндокринологической клиники, занимающейся лечением, в том числе и хирургическим, различной патологии щитовидной железы. Данные, сообщенные различными авторами, свидетельствуют об увеличении частоты рака в так называемых узловых образованиях щитовидной железы. Н.М. Амирова, Т.Б. Дубошина (2003) опубликовали данные, включающие результаты 1749 операций по поводу рака щитовидной железы в 1951—2002 гг. в клинике Куйбышевской медицинской академии. Если в 80-х гг. ХХ в. рак обнаруживался у каждого десятого больного из оперированных по поводу зоба, то в 2002 г. рак выявлен уже у каждого шестого. Рак щитовидной железы составляет 1—1,5% от всех злокачественных новообразований в мире.
По данным ВОЗ, за последние 20 лет заболеваемость раком щитовидной железы в мире удвоилась, главным образом — за счет заболевания лиц молодого и среднего возраста. В последние годы наблюдается значительное увеличение общей патологии щитовидной железы, на фоне которой соответственно возрастает число случаев опухолевых поражений. Особенно это касается детей, живущих в регионах, пострадавших в результате аварии на Чернобыльской АЭС. У взрослых частота общей патологии щитовидной железы в этих районах также возросла. Так, по данным Р.В. Аристархова с соавт. (2003), в Рязанской области количество больных аутоиммунным тиреоидитом возросло к 2000 г. по сравнению с 1985 г. (до Чернобыльской аварии) в 14,4 раза, узловым коллоидным зобом — в 8 раз, аденомой в сочетании с аутоиммунным тиреоидитом и множественными аденомами — в 40 раз.
Вопрос взаимосвязи рака щитовидной железы с фоновыми процессами является одним из основных в онкологии. Сведения по данной проблеме противоречивы. Так, в Казахстане в очагах эндемического зоба рак щитовидной железы наблюдается в 10—15 раз чаще, чем в неэндемических районах. По-видимому, увеличение заболеваемости обусловлено не только истинным ее приростом, но и лучшей диагностикой, благодаря совершенствованию диагностических методов, созданию профильных диагностических отделений.
О.Н. Зинкевич с соавт. (2003), приводят данные о лечении больных раком щитовидной железы в Ростовской клинической больнице. Они считают, что в 42,8% фоновым заболеванием, при котором развился рак, является аутоиммунный тиреоидит, в 27,9% — многоузловой коллоидный зоб, в 3,6% — диффузный токсический зоб и в 1,2% — подострый тиреоидит.
Установлено, что основной причиной гиперплазии щитовидной железы служит дефицит йода в организме. Обычно такая гиперплазия является компенсаторной, но иногда становится необратимой. Гиперпластическому процессу могут способствовать также факторы, блокирующие синтез тиреоидных гормонов. Таким образом, развитию злокачественных опухолей щитовидной железы нередко предшествуют узловой зоб, диффузная гиперплазия тиреоидной паренхимы обратимого и необратимого характера, узловая гиперплазия, аденомы.
Непрерывный рост информации о строении и функции органов и тканей, о гисто— и морфогенезе возникающих из них опухолей, вызывает необходимость пересмотра и усовершенствования классификации новообразований.
Исследования, проведенные в 70—80 гг. ХХ в., привели к принципиально новому представлению о структурно-функциональной организации щитовидной железы. Щитовидную железу рассматривают как орган, в котором многогранная функциональная деятельность разделена между самостоятельными клеточными группами. Это фолликулярные, или А—клетки, вырабатывающие тироксин; В—клетки (клетки Ашкенази), накапливающие серотонин и являющиеся не дистрофическими, а, напротив, обладающие высокой метаболической активностью; парафолликулярные, или С—клетки, синтезирующие кальцитонин.
Таким образом, опровергнуто мнение о едином гистогенезе опухолей щитовидной железы, связанных, как считалось ранее, только с фолликулярными клетками. Полученные сведения потребовали пересмотра и критической оценки многочисленных систематизаций рака щитовидной железы, предложенных большим числом авторов и выработки единой классификации.
В 1980 г. опубликована Международная гистологическая классификация опухолей щитовидной железы №11, разработанная группой экспертов ВОЗ (Hedinger Сh., Soben Z.).
Классификация опухолей щитовидной железы
А. А-клетки (фолликулярные).
А.1. Доброкачественные:
А.1.1. фолликулярная аденома;
А.1.2. папиллярная аденома;
А.1.3. трабекулярная аденома.
А.2. Злокачественные:
А.2.1. фолликулярная аденокарцинома;
А.2.2. папиллярная аденокарцинома;
А.2.3. недифференцированный рак.
B. B-клетки (клетки Ашкенази).
B.1. Доброкачественные:
B.1.1. фолликулярная аденома;
B.1.2. папиллярная аденома;
B.1.3. трабекулярная аденома.
B.2. Злокачественные:
B.2.1. фолликулярная аденокарцинома
B.2.2. папиллярная аденокарцинома;
B.2.3. недифференцированный рак.
C. C-клетки (парафолликулярные).
C.1. Доброкачественные:
С.1.1. сóлидная аденома.
C.2. Злокачественные:
С.2.1. сóлидный рак с амилоидозом стромы (медуллярный).
D. Метаплазированный эпителий.
D.2. Злокачественные:
D.2.1. плоскоклеточный рак;
E. Неэпителиальные клетки.
E.1. Доброкачественные:
E.1.1. фиброма;
E.1.2. леймиома;
E.1.3. гемангиома;
E.1.4. тератома.
E.2. Злокачественные:
E.2.1. лимфосаркома;
E.2.2. ретикулосаркома;
E.2.3. фибросаркома;
B.2.4. гемангиоэндотелиома;
B.2.5. гемангиоперицитома.
F. Эпителиальные и неэпителиальные клетки.
F.1. Доброкачественные:
F.1.2. неклассифицируемые опухоли.
Примечание:
1. Разновидности фолликулярных аденокарцином — опухоль Ланганса и так называемая метастазирующая аденома.
2. Одна из разновидностей папиллярной аденокарциномы — склерозирующая микрокарцинома, она изредка может иметь строение других форм опухолей щитовидной железы.
3. Первичные доброкачественные и злокачественные опухоли, которые по гистологическому строению не укладываются ни в одну из указанных категорий.
Эта классификация разработана коллективом авторов ГУ РОНЦ им. Н.Н. Блохина РАМН во главе с академиком РАМН Н.А. Краевским. Опубликованная в виде методических рекомендаций в 1976 г. классификация, в принципе, соответствует Международной гистологической классификации.
В 1989 г. в журнале Саncer опубликовано 2 издание гистологической классификации, разработанной группой экспертов ВОЗ (Sobin Z., 1989). Классификация включает в себя основные формы опухолей и удобна для практического применения.
А. Доброкачественные.
I. Эпителиальные опухоли.
1. Фолликулярная аденома.
2. Другие.
Б. Злокачественные.
1. Фолликулярный рак.
2. Папиллярный рак.
3. Медуллярный рак.
4. Недифференцированный (анапластический) рак.
5. Другие.
II. Неэпителиальные опухоли.
III. Злокачественные опухоли.
IV. Смешанные опухоли.
V. Вторичные опухоли.
VI. Неклассифицируемые опухоли.
VII. Опухолеподобные поражения.
Клинико-морфологическая характеристика опухолей
А. Эпителиальные опухоли
I. Рак из А—клеток является наиболее распространенным:
1. Чаще всего встречается папиллярная аденокарцинома (по нашим данным, 77,7% ). Соотношение заболевших мужчин и женщин составляет 1:2, средний возраст — 46 лет. Для папиллярного рака характерна высокая частота регионарного метастазирования. Эта форма рака развивается медленно, поэтому существующая 5—10 лет в щитовидной железе опухоль может быть злокачественной с начала своего формирования. Нередко аденома и рак щитовидной железы встречаются одновременно, но независимо друг от друга. У 13% пациентов интраоперационно выявляется инвазия опухоли в окружающие ткани. Отдаленные метастазы выявляются у 3% пациентов. Гистологическое строение опухоли часто неоднородно, так, наряду с папиллярным встречаются фолликулярные и сóлидные структуры, соотношение которых между собой значительно варьирует. Клиническую картину заболевания определяет наличие в опухоли папиллярных структур.
2. Значительно реже встречается фолликулярная аденокарцинома. В наших наблюдениях она выявлена у 3% больных. Женщины болеют чаще, соотношение с мужчинами 9,3:1. Средний возраст больных 46 лет. Опухоль развивается медленно и длительное время остается локализованной. Регионарные метастазы встречаются значительно реже, чем при папиллярном раке. Отдаленные метастазы реализуются чаще (10% случаев). При гистологическом исследовании опухоль представлена как фолликулярными и трабекулярными структурами, так и сóлидными разрастаниями опухолевых клеток, но не содержит папиллярных структур. Гистологически — микрофолликулярное строение, характерен инвазивный рост в капсулу опухоли и/или кровеносные сосуды, что значительно ухудшает прогноз заболевания.
3. Недифференцированный рак на нашем материале встретился в 3% случаев. Соотношение мужчин и женщин примерно одинаково, средний возраст — 53,5 лет. Клиническое течение этой формы рака чрезвычайно быстрое, наблюдается бурный рост первичной опухоли, реализация регионарных и отдаленных метастазов. Микроскопически картина неоднородна, опухоль состоит как из мелких, так и из крупных клеток, может иметь веретеноклеточное строение.
Изучение структуры рака щитовидной железы в сопоставлении с клиническими данными позволило в 2,3% случаев выявить трансформацию дифференцированных форм опухоли (папиллярной и фолликулярной аденокарцином) в недифференцированные. Бурный рост опухоли свидетельствует о дедифференцировке клеток и указывает на наличие низкодифференцированного рака. Указанные данные свидетельствуют в пользу активной хирургической тактики при узловых образованиях щитовидной железы.
II. Рак из В—клеток (клеток Ашкенази) встречается крайне редко.
А.И. Пачес и Р.М. Пропп, обладающие опытом лечения 1360 больных раком щитовидной железы, встретили лишь 19 пациентов с такой формой опухоли. Существует мнение о том, что опухоль из клеток Ашкенази более 4 см — с бóльшей вероятностью злокачественная.
III. Рак из С—клеток (сóлидный с амилоидозом стромы или медуллярный рак).
В отечественной литературе эта форма рака впервые описана Д.Г. Заридзе и Р.М. Пропп в 1968 г. В настоящее время рассматривается принадлежность С— и В—клеток к APUD—системе.
Медуллярный рак щитовидной железы наблюдается как спорадически, так и при эндокринном семейном синдроме. В 1961 г. Sipple G. показал, что возникновение рака щитовидной железы у больных феохромоцитомой встречается в 14 раз чаще, чем в целом по населению. Синдром Сиппла характеризуется наличием медуллярного рака щитовидной железы, феохромоцитомы, гиперплазии или аденомы паращитовидных желез, марфаноидного фенотипа, ганглионейроматоза ЖКТ. При этой форме рака соотношение женщин и мужчин составляет 4:1, средний возраст больных 50 лет.
Медуллярный рак щитовидной железы занимает промежуточное положение между дифференцированными и недифференцированными новообразованиями. Эта форма рака гормонально активна, раковые клетки способны вырабатывать кальцитонин, что свидетельствует об их достаточной зрелости и объясняет относительно медленное течение болезни. По данным литературы, одним из характерных признаков медуллярного рака является диарея, обусловленная действием гуморальных факторов, которые секретируются опухолью (4,7% случаев по данным Р.М. Пропп).
Опухоль имеет тенденцию к прогрессирующему росту. Регионарные метастазы наблюдаются часто — 60—80% случаев, отдаленные — в 30%. При гистологическом исследовании препарата медуллярного рака могут быть обнаружены мелкие округлые или вытянутые клетки, содержащие аморфные массы амилоида; иногда встречаются веретенообразные клетки. Следует подчеркнуть трудность диагностики медуллярного рака, наиболее часто принимаемого за недифференцированный рак или параганглиому.
Увеличение концентрации кальцитонина позволяет рано, часто до клинических признаков, диагностировать медуллярный рак щитовидной железы, особенно в семьях повышенного генетического риска.
Плоскоклеточный рак составляет 1—3% всех злокачественных опухолей щитовидной железы. Гистологически многослойный плоский эпителий в щитовидной железе связан с остатками эмбриональных клеточных элементов щитовидно-язычного протока. Чаще плоскоклеточный рак щитовидной железы образуется в результате плоскоклеточной метаплазии тиреоидного эпителия. Встречается эта форма рака чаще у людей пожилого возраста (60 лет и более). Уже при первичном обращении, как правило, имеет место распространенная форма опухоли. Микроскопически опухоль имеет типичное строение плоскоклеточного рака.
<
Б. Неэпителиальные опухоли
Неэпителиальные опухоли встречаются редко. Их клиническое течение не отличается от развития опухолей соответствующего генеза в других органах и тканях. Саркомы щитовидной железы отличаются высокой степенью злокачественности.
Особенности клинического течения опухолей
В прогностическом плане необходимо отметить три наиболее важных фактора: возраст пациента, пол, стадия распространенности опухолевого процесса.
Возраст
Большинство исследователей сообщают, что возраст является важным прогностическим фактором, отражающим смертность от рака щитовидной железы. Установлено, что смертность от рака щитовидной железы значительно выше при возрасте пациентов старше 40 лет и прогрессирующе увеличивается с каждым последующим десятилетием, достигая наиболее высоких цифр у пациентов старше 60 лет. Иное соотношение наблюдается при анализе рецидивов заболевания. Наибольшая частота рецидивов отмечена в возрасте до 40 лет и старше 60 лет. Это один из наиболее серьезных аргументов за агрессивную тактику лечения пациентов указанных возрастных групп с целью снижения числа рецидивов рака щитовидной железы, особенно у детей и людей молодого возраста.
Пол
Прогноз при раке щитовидной железы более благоприятен у женщин, чем у мужчин, но это различие является незначительным. Во многих исследованиях было установлено, что пол является независимым фактором, не влияющим на выживаемость пациента. Однако учитывая, что смертность от рака щитовидной железы у мужчин в 2 раза выше, чем у женщин, любой мужчина старше 40 лет, имеющий рак щитовидной железы, должен находиться под пристальным динамическим наблюдением после лечения.
Распространенность
Для рационального лечения и суждения о прогнозе важно иметь сведения не только о гистологическом строении и клиническом течении опухоли, но и о ее распространенности. Последние оцениваются по стадиям и символам ТNM.
В 2002 г. опубликована новая классификация рака щитовидной железы по системе ТNM. По сравнению с 5 изданием (1997), в новой классификации к символу Т1 отнесены опухоли размером до 2 см, что более логично, т.к. узловые образования щитовидной железы размером до 1 см пропальпировать весьма сложно, если они не располагаются в перешейке. Также дано более четкое понятие для опухолей, соответствующих Т3 — Т4. Так, при опухоли, соответствующей Т3, имеется минимальное распространение рака за капсулу железы с распространением на грудино-щитовидную мышцу, щито-перстневидную мембрану. Категория Т4 разделена на 2 подкатегории — Т4A и Т4B. К первой отнесены опухоли с прорастанием подкожно в мягкие ткани, гортань, трахею, пищевод, возвратный нерв, т.е. все резектабельные случаи рака щитовидной железы. Ко второй группе отнесены случаи условно местно нерезектабельные, т.е. с распространением на предпозвоночную фасцию, сосуды средостения, с окклюзией общей сонной артерии.
Также произошли изменения в оценке символов N1A и N1B, последние оптимизированы. Так, к N1A отнесены пораженные лимфатические узлы первого этапа метастазирования: пара— и претрахеальные, предгортанные. К N1B — пораженные шейные лимфатические узлы второго этапа метастазирования: глубокие яремные лимфатические узлы на стороне поражения, на противоположной стороне, с обеих сторон, а также лимфатические узлы передневерхнего средостения.
При большинстве сóлидных злокачественных опухолей прогностическая важность лимфогенного метастазирования хорошо известна и включена в принятую систему стадирования. В отличие от других злокачественных опухолей, прогностическая значимость метастатического поражения лимфатических узлов при раке щитовидной железы и их оптимальное лечение продолжают оставаться предметом дискуссии.
Определить действительную частоту метастазов нелегко, ибо диагностика их различна в клинике и в патологоанатомическом отделении. В первом случае распознаются метастазы главным образом в лимфатических узлах, легких и костях, во втором, помимо указанных локализаций, — в органах брюшной полости и в других областях. Поэтому сведения о частоте метастазов рака щитовидной железы зависят не только от состояния больных во время их обследования, но и качества диагностики — как на клинической стадии, так и на патолого-анатомической. Этим и объясняется следующий факт: соотношение больных без метастазов и с метастазами в сообщениях различных авторов резко различаются. По патолого-анатомическим данным, метастазы наблюдаются в 89% случаев, а по клиническим данным — в 33,7% случаев.
Критерий Т (первичная опухоль щитовидной железы)
Все категории могут быть разделены на (A) — солитарные опухоли, (B) — многофокусные опухоли (наибольший размер образования определяет стадию).
ТX — первичная опухоль не может быть оценена;
Т0 — нет признаков первичной опухоли;
Т1 — опухоль 2 см или меньшего диаметра, ограничена щитовидной железой;
Т2 — опухоль больше 2 см, но не более 4 см, также ограничена пределами капсулы щитовидной железы;
Т3 — опухоль более 4 см, ограничена щитовидной железой, или любая опухоль с минимальным распространением за капсулу щитовидной железы (распространение в грудино-щитовидную мышцу, или в мягкие ткани около щитовидной железы);
Т4A — опухоль любого размера, распространяющаяся за капсулу щитовидной железы, проникающая в подкожные мягкие ткани, гортань, трахею, пищевод или поражающие возвратный нерв;
Т4B — опухоль, инфильтрирующая превертебральную фасцию, или случаи вовлечения сонной артерии или сосудов средостения.
Все формы анапластического рака расцениваются как Т4
Т4A — интратиреоидная анапластическая опухоль, хирургически резектабельная;
Т4B — экстратиреоидная анапластическая опухоль, хирургически нерезектабельная.
Критерий N (регионарные лимфатические узлы)
Регионарные лимфатические узлы центральных отделов, латеральные, шейные и верхние медиастинальные.
NX — регионарные лимфатические узлы не могут быть оценены;
N0 — нет регионарных метастазов;
N1 — регионарные метастазы;
N1A — метастазы 1 уровня метастазирования: претрахеальные, паратрахеальные и преларингеальные (дельфиниев узел);
N1B — метастазы в гомолатеральные, двухсторонние или контралатеральные шейные или верхние медиастинальные лимфатические узлы.
Критерий М (отдаленные метастазы)
М1 — отдаленные метастазы не могут быть обнаружены;
М0 — нет отдаленных метастазов;
М1 — есть отдаленные метастазы.
Стадирование
Рекомендуется отдельное стадирование для папиллярного или фолликулярного рака, для медуллярного и анапластического (недифференцированного рака).
Таблица 1
| Папиллярный или фолликулярный рак | |||
| До 45 лет | |||
| Стадия I | Любая Т | Любая N | M0 |
| Стадия II | Любая Т | Любая N | М1 |
| 45 лет и старше | |||
| Стадия I | Т1 | N0 | M0 |
| Стадия II | T2 | N0 | M0 |
| Стадия III | T3 | N0 | M0 |
| T1 | N1A | M0 | |
| T2 | N1A | M0 | |
| T3 | N1A | M0 | |
| Стадия IVA | Т4A | N0 | M0 |
| Т4A | N1A | M0 | |
| Т1 | N1B | M0 | |
| Т2 | N1B | M0 | |
| Т3 | N1B | M0 | |
| Т4A | N1B | M0 | |
| Стадия IVB | T4B | Любая N | M0 |
| Стадия IVC | Любая Т | Любая N | М1 |
| Медуллярный рак | |||
| Стадия I | T1 | N0 | M0 |
| Стадия II | T2 | N0 | M0 |
| Стадия III | T3 | N0 | M0 |
| T1 | N1A | M0 | |
| T2 | N1A | M0 | |
| T3 | N1A | M0 | |
| Стадия IVA | T4A | N0 | M0 |
| T4A | N1A | M0 | |
| T1 | N1B | M0 | |
| T2 | N1B | M0 | |
| T3 | N1B | M0 | |
| T4A | N1B | M0 | |
| Стадия IVB | T4B | Любая N | М0 |
| Стадия IVC | Любая Т | Любая N | M1 |
| Анапластический рак | |||
| Все формы анапластического рака рассматриваются как IV стадия |
|||
| Стадия IVA | T4A | Любая N | M0 |
| Стадия IVB | T4B | Любая N | M0 |
| Стадия IVC | Любая Т | Любая N | M1 |
Установлена определенная зависимость между морфологической формой опухоли и характером метастазирования. Так, папиллярная аденокарцинома метастазирует преимущественно в регионарные лимфатические узлы; фолликулярная аденокарцинома имеет тенденцию к более частому гематогенному распространению; недифференцированный рак обладает высокой способностью и лимфогенного, и гематогенного метастазирования. Так, по данным Клиники Мейо, имеющей 60-летний опыт лечения рака щитовидной железы и обладающей материалом о 3048 больных с дифференцированными формами рака щитовидной железы, регионарные метастазы выявлены у 40% пациентов. Данные о регионарном метастазировании указанных опухолей, приводимые авторами прежних лет, свидетельствовали о более высоких показателях регионарного метастазирования (60—80%).
При анализе частоты метастазирования необходимо учитывать:
— гистологическое строение и гистогенез опухоли,
— характер ее роста и распространенность процесса,
— длительность заболевания,
— пол,
— возраст больных.
Исследования, проведенные Р.М. Пропп в 60—70 гг. ХХ в., показали, что папиллярные аденокарциномы из А— и В—клеток метастазируют в регионарные лимфатические узлы чаще, чем фолликулярные аденокарциномы из этих же клеток. Однако отдаленные метастазы чаще наблюдаются у больных фолликулярной аденокарциномой из А—клеток. Метастазирование зависит и от структуры одной и той же опухоли: оно чаще происходит при папиллярной аденокарциноме из А—клеток с наличием сóлидного и недифференцированного компонентов. Такая форма рака обнаружена у всех больных с отдаленными метастазами и у 56,8% больных с регионарными метастазами. Наибольшая частота регионарного метастазирования выявлена при медуллярном раке, а двухсторонние метастазы более часты при дифференцированном раке из А— и В—клеток. Регионарные метастазы чаще возникают при расположении опухоли в пределах щитовидной железы. Этот несколько необычный факт авторы объясняют биологическими особенностями опухолей данного вида, наличием среди них большого числа скрытых форм рака щитовидной железы (38,3% случаев). Именно для последних характерно внутрижелезистое распространение опухоли с обширным регионарным метастазированием.
Для медуллярного рака метастазы в регионарных лимфатических узлах при внутрижелезистом расположении опухоли выявляются несколько чаще, чем при ее инфильтрирующем росте. По-видимому, это также связано с наличием среди больных лиц со скрыто протекающими формами рака (16,6% случаев).
При раке щитовидной железы не отмечено роста регионарного метастазирования при бóльшей длительности болезни. Даже при анамнезе данного заболевания 5 лет и более, почти у 30% больных регионарные метастазы не реализованы. Для рака щитовидной железы характерно множественное развитие метастазов во всех регионарных лимфатических коллекторах, однако наиболее часто поражаются лимфатические узлы глубокой яремной цепи: верхние — 93,8%, средние — 88,19%, нижние — 95,3%. Кроме того, высока вероятность поражения лимфатических узлов передневерхнего отдела средостения (56,8%), а также паратрахеальных (47,3%).
При раке щитовидной железы у больных в возрасте до 40 лет регионарные метастазы наблюдались чаще (70% случаев), а отдаленные реже (3,4% случаев), чем в возрасте после 40 лет (соответственно 64 и 7% случаев), в основном за счет преобладания больных с дифференцированными опухолями.
У женщин и регионарные, и отдаленные метастазы возникают реже, чем у мужчин, что также можно объяснить преобладанием у них дифференцированных форм рака. У женщин в возрасте до 40 лет чаще выявляются регионарные и реже — отдаленные метастазы. После 40 лет частота первых уменьшается, а вторых — увеличивается. У мужчин в обеих возрастных группах отмечено более тяжелое течение болезни. Отдаленные метастазы — основная причина смерти при дифференцированных формах рака щитовидной железы. Почти у 10% пациентов с папиллярным раком и у 25,5% с фолликулярным имеются отдаленные метастазы. Отдаленные метастазы встречаются чаще среди форм рака из клеток Ашкенази (35%) и у пациентов старше 40 лет. При изучении характера отдаленного метастазирования установлено: легкие поражаются в 49% случаев, кости — в 25%, сочетанное поражение легких и костей — в 15%, головной мозг и мягкие ткани поражаются в 10% случаев.
Вместе с тем следует отметить особенности метастазирования в тот или иной орган. Так, при метастазировании рака щитовидной железы в легкие очень часто наблюдается распространение опухолевого процесса в другие органы и ткани и прежде всего в средостение. С другой стороны, метастазы в лимфатические узлы шеи и в кости очень редко сопровождаются метастазированием в легкие.
Метастазы в легкие при рентгенологическом исследовании обычно имеют вид крупно-, средне— и мелкоочаговых теней, реже — единичных округлых образований. В первом случае они напоминают картину милиарного диссеминированного туберкулеза. При этом, несмотря на обширность поражения легочной ткани, обычно отсутствуют признаки нарушения легочной вентиляции. Такие больные длительное время лечатся по поводу предполагаемого туберкулеза.
Для метастазов рака щитовидной железы в кости характерно их медленное прогрессирование. По данным литературы известно, что поражаемость отдельных костей метастазами рака щитовидной железы следующая (в порядке убывания): кости черепа, позвоночник, грудина, ребра, кости таза и конечности.
Метастазы рака щитовидной железы во внутренние органы обнаруживаются редко и, в основном, во время аутопсии. Но внедрение РКТ, МРТ и УЗКТ позволяет в большинстве случаев выявить отдаленные метастазы прижизненно.
Вероятность выживания наиболее высока среди молодых пациентов как с диффузными рентген-негативными метастазами в легкие, выявленными при сцинтиграфии с 131I, так и с рентген-позитивными метастазами.
Несмотря на имеющиеся достижения в разработке и оптимизации лечебной тактики и техники операций на щитовидной железе при различных видах рака, частота послеоперационных рецидивов, по литературным данным, не снижается, составляя 15—30% при дифференцированных и 60—80% при недифференцированных новообразованиях.
По данным МНИИОИ им. П.А. Герцена, на основе анализа данных о 106 больных с рецидивами рака щитовидной железы, выявлено: так называемые ранние рецидивы, возникающие через 1—3 года после операции, составляют 41,5%; поздние рецидивы, реализующиеся через 3 года и более, встречаются в 58,5% случаев. У 14% пациентов рецидив рака щитовидной железы обнаружен через 10 и более лет после хирургического вмешательства.
Анализ причин появления рецидивов рака щитовидной железы показал, что в подавляющем большинстве случаев (90,6%) этим больным были произведены так называемые экономные операции. Причем большинству выполнены операции следующего объема: энуклеация узла, энуклеация — резекция доли, частичная резекция доли, удаление перешейка, субфасциальная или субтотальная резекция доли. Таким образом, одной из основных причин рецидива рака щитовидной железы следует считать нерадикальность первично выполненной операции.
По данным Клиники Мейо (Hay I.D., Grant et al., 1988), существует достоверная связь между развитием местного рецидива и тремя показателями: возраст пациента — 60 лет и старше, размер опухоли — 4 см или более, а также выход опухоли за пределы щитовидной железы. Наличие регионарных метастазов на момент диагностики опухоли не повышает риск местного рецидива.
При анализе причин появления так называемых поздних рецидивов рака щитовидной железы следует, по-видимому, учитывать биологические особенности опухоли, медленное прогрессирование дифференцированных форм рака. Рецидив рака щитовидной железы протекает, как правило, более злокачественно, чем первичная опухоль той же структуры. Эта злокачественность выражается как клинически, так и морфологически.
Помимо изменения биологических свойств опухоли, здесь следует подчеркнуть и трудности диагностики рецидивной опухоли, бессимптомность течения, приводящие к инфильтрации окружающих тканей (передних длинных мышц шеи, трахеи, пищевода), что значительно ухудшает прогноз заболевания.
Морфологическая структура рецидивной опухоли отличается от первичного рака щитовидной железы снижением степени дифференцировки новообразования и, следовательно, повышением степени злокачественности. Если при первичной операции дифференцированная структура опухоли щитовидной железы отмечена в 76% случаев, то при повторном хирургическом вмешательстве — в 61% случаев (Демидов В.П. и др., 1978 г.).
Исходя из изложенных фактов, следует подчеркнуть, что необходимо тщательно и в течение длительного времени следить за состоянием оставшейся части железы, зон регионарного метастазирования, а также внутренних органов.
Своеобразно протекающие формы рака щитовидной железы
Рак щитовидной железы характеризуется многообразием форм и клинических проявлений. К ним относятся своеобразно текущие формы рака щитовидной железы. Одними из них являются микрокарциномы или скрыто текущие формы рака щитовидной железы. По мнению большинства авторов, таковыми являются формы рака менее 1 см в диаметре, т.е. клинически не определяемые. Первым клиническим признаком проявления таких форм рака в 90% случаев являются регионарные метастазы. В остальных наблюдениях эти формы рака обнаруживаются после удаления доброкачественных образований щитовидной железы (аденомы, зоба), при плановом гистологическом исследовании. Исключительно редко первым проявлением скрыто текущего рака являются отдаленные метастазы. Диагностика этих опухолей очень сложна, нет единого мнения, опухоли какого размера относить к микрокарциномам. Одни авторы считают, что это опухоли размером до 0,5 мм в диаметре, другие — новообразования до 1,5 см в диаметре.
M. Zanaret et al. (1998) в обзорной статье, касающейся микрокарцином щитовидной железы, разделили пациентов на 2 группы. Первую группу составили больные с опухолями менее 5 мм в диаметре, вторую — с опухолями более 5 мм в диаметре.
Для опухолей первой группы характерно:
— наличие капсулы,
— отсутствие мультицентрического роста и регионарных метастазов.
Во второй группе опухоли были схожи с новообразованиями больших размеров.
Как и при других формах рака щитовидной железы, скрытый рак этого органа чаще отмечается у женщин, чем у мужчин. Средний возраст больных составляет 45 лет.
Скрыто протекающий рак характеризуется медленным течением, при этом первичная опухоль не определяется, а на первый план в клинической картине болезни выходят регионарные метастазы и, значительно реже, — отдаленные. Особенностью этих опухолей является длительное развитие метастазов в лимфатических узлах шеи, которые нередко могут достигать больших размеров при неопределяемой первичной опухоли в щитовидной железе.
Следует отметить, что место расположения первичной опухоли в щитовидной железе во многом определяет возможность ее обнаружения. Так, при локализации опухоли в центре доли, ближе к задней ее поверхности, а также у трахеи, в области верхнего или нижнего полюса доли, она недоступна для пальпации. Если же опухоль расположена поверхностно, в перешейке или пирамидальной доле (а также у лиц астенического сложения), она может быть доступна пальпации даже при небольших размерах (до 1 см в диаметре).
Отдаленные метастазы при скрыто протекающем раке встречаются редко. Однако при недостаточном знакомстве врачей с данной патологией могут быть трагические ошибки. Так, у одной нашей больной 41 года на боковой поверхности шеи выявлен метастаз папиллярной аденокарциномы. По поводу неправильно поставленного диагноза рака яичников (РЯ) по месту жительства сделана резекция яичников, в которых опухоли не обнаружено. Затем произведена операция Крайла и проведена лучевая терапия в суммарной очаговой дозе 40 Гр. Лишь после этого больная была направлена в ГУ РОНЦ им. Н.Н. Блохина РАМН, где при пересмотре препаратов обнаружены клетки папиллярного рака щитовидной железы. Клинически опухоль в щитовидной железе не определялась, но больной выполнена субтотальная резекция щитовидной железы. Только при послеоперационном гистологическом исследовании была обнаружена склерозирующая микрокарцинома в гомолатеральной по отношению к удаленному метастазу доле щитовидной железы.
Данное наблюдение поучительно с нескольких позиций. Неправильная диагностика привела к неправильной тактике лечения, энуклеации лимфатического узла и операции на яичниках у сравнительно молодой женщины, а также облучению шеи. Последнее в таких случаях неэффективно и не показано. Выявлению первичного очага в щитовидной железе должно способствовать гистологическое исследование метастазов в лимфатические узлы шеи, но это с диагностической точки зрения имеет значение только при достаточной осведомленности врачей различного профиля, к которым попадают больные, об особенностях скрытого рака щитовидной железы. В связи с изложенным, наиболее ценными являются данные А.И. Пачес и Р.М. Пропп (1995), которые выделяют 3 основные группы больных скрытым раком:
— больные, у которых опухоль щитовидной железы заподозрена до операции (32%);
— больные, у которых опухоль щитовидной железы обнаружена макроскопически во время операции (36%);
— больные, у которых опухоль щитовидной железы выявлена только после гистологического исследования (36%). Множественные очаги рака у больных мужчин выявлены в 38%, у женщин — в 20% случаев.
Большинство авторов считают, что скрытый рак щитовидной железы имеет папиллярное, папиллярно-фолликулярное и реже — фолликулярное строение. Однако исследования Р.М. Пропп 1971—1973 гг. показали возможность существования всех морфологических форм рака щитовидной железы из А—, В— и С— клеток при скрытом раке этого органа.
Вопрос о скрытом раке щитовидной железы тесно переплетается с проблемой опухолей т.н. аберрантных (добавочных) щитовидных желез. В прежние годы понятие первичной злокачественной опухоли, развивающейся в добавочных щитовидных железах, было распространено широко. Сторонниками тезиса о существовании доброкачественных и злокачественных опухолей в боковых добавочных щитовидных железах в 60—70—е гг. ХХ в. были известные французские авторы M. Dargent и G. Gricouroff. Последний обнаружил ткань щитовидной железы в лимфатических узлах шеи. Большое число сторонников этого мнения было и среди отечественных авторов. Однако, благодаря тщательным исследованиям того же периода, эта точка зрения большинством ученых отвергнута.
Следует отметить, что из-за неправильной трактовки сущности заболевания применялись и неадекватные методы лечения. Например, при операции по поводу так называемых боковых абберантных струм щитовидная железа оставлялась на месте, и в большинстве случаев даже не подвергалась ревизии во время операции на боковой поверхности шеи. Таким образом чаще всего удалялись регионарные метастазы (и то нерадикально), а первичный очаг рака в щитовидной железе оставлялся. В дальнейшем судьба этих больных не прослеживалась.
Развитие большого рака в дистопированных боковых щитовидных железах наблюдается очень редко, а маленький, скрыто протекающий рак, как было показано, возникает достаточно часто.
Поэтому практически все опухолевые узлы на боковой поверхности шеи, имеющие структуру щитовидной железы, следует рассматривать как метастатические.
Среди редко встречающихся образований, связанных с пороками развития щитовидной железы, следует отметить зоб корня языка, иногда с полной эктопией железы, внутригрудной зоб, рак из остатков щитоязычного протока.
Комплексная диагностика опухолей
По клиническому течению дифференцированные формы новообразований щитовидной железы, составляющие наибольший процент рака этого органа, как правило, являются бессимптомными в течение длительного времени и макроскопически представляют собой обычный узел в щитовидной железе. Оценка злокачественности данных узлов при физикальном исследовании представляет значительные трудности. Доброкачественные и злокачественные узлы щитовидной железы в своем большинстве являются бессимптомными. Длительное развитие и течение дифференцированных аденокарцином щитовидной железы часто ведет к поздней диагностике, что, в свою очередь, ухудшает результаты лечения. Вместе с тем существует ряд анатомических и клинических признаков, позволяющих заподозрить наличие рака щитовидной железы. Так, по данным Н.С. Кузнецова с соавт. (2003), вероятность, что узел является злокачественным, увеличивается в 7 раз, если имеются следующие клинические признаки:
— плотный узел; узел, фиксированный к соседним анатомическим структурам;
— узел в щитовидной железе, сочетающийся с увеличенными регионарными лимфатическими узлами;
— узел, сочетающийся с параличом голосовой складки;
— быстрорастущий узел.
Если два и более из этих признаков выявлены у пациента, вероятность рака щитовидной железы достигает 100%.
Однако данные, приводимые в последние годы, свидетельствуют о слабом прогрессе в диагностике рака щитовидной железы.
Между тем число больных с узловыми поражениями щитовидной железы достаточно велико, и они продолжают наблюдаться у терапевтов и эндокринологов в противозобных кабинетах, созданных в тот период, когда на первом месте стояла проблема борьбы с эндемическим зобом. Именно эти больные, годами наблюдаемые данными специалистами, являются группами повышенного риска возникновения у них рака щитовидной железы. Так, по данным В.П. Демидова с соавт., среди 338 больных, оперированных по поводу узловых образований в щитовидной железе, в 31,4% случаев был обнаружен рак.
В клинике ГУ РОНЦ им. Н.Н. Блохина РАМН применяется диагностический комплекс, включающий помимо клинического обследования (анамнез, осмотр, пальпация), следующие методы: УЗКТ щитовидной железы, пункцию опухоли щитовидной железы и регионарных метастазов, которая при необходимости (чаще при скрыто протекающем раке или при увеличенных регионарных лимфатических узлах небольших размеров) проводится под контролем УЗКТ; рентгенологическое исследование; сцинтиграфию с радиактивным йодом (131 I). Всем больным производится ларингоскопия, с помощью которой можно определить подвижность голосовых складок. В последние 20 лет широкое применение получили РКТ и МРТ, которые используются как для диагностики опухолей небольших размеров, так и при распространенных новообразованиях для определения истинных границ поражения.
Ошибочной интерпретации в диагностике опухолей способствует бытующее среди врачей общей лечебной сети мнение о том, что злокачественные опухоли всегда быстрорастущие, с коротким анамнезом. Между тем по сводным данным Р.М. Пропп, оказалось, что со времени выявления опухоли щитовидной железы до начала лечения проходит значительный срок: 5 лет и более у 36% больных. Кроме того, врачи привыкли думать о том, что рак возникает преимущественно у лиц пожилого возраста. Однако, как показали приведенные ранее данные, рак щитовидной железы нередко встречается у молодых людей.
В последние годы стали применять радиоиммунологический метод определения тиреоглобулина (ТГ) в сыворотке крови у больных с дифференцированными формами рака щитовидной железы (95% этих форм рака щитовидной железы синтезируют ТГ). При генерализованном метастазировании отмечается очень высокий уровень ТГ, а при регионарных метастазах он незначительно повышен или нормальный. Однако высокий уровень ТГ наблюдается и при доброкачественных процессах в щитовидной железе, при гипертиреозе.
Лабораторные данные имеют ведущее значение при медуллярном раке щитовидной железы. При этой форме рака происходит увеличение секреции кальцитонина. Определение содержания кальцитонина в периферической крови имеет большое значение для суждения о степени радикальности выполненной операции при медуллярном раке, а также при динамическом наблюдении за больными с целью выявления рецидива и метастазов этого рака. В случае радикальной операции уровень кальцитонина резко падает, а значительное увеличение этого показателя свидетельствует о рецидиве и метастазах.
С помощью УЗКТ появилась возможность выявлять небольшие (до 1 см в диаметре) узлы в щитовидной железе. Это имеет большое значение для диагностики скрытого рака щитовидной железы, а также для выявления небольших непальпируемых лимфатических узлов на шее.
Следует, однако, отметить, что при использовании УЗКТ велика вероятность гипердиагностики как первичных опухолей щитовидной железы, так и регионарных метастазов. Поэтому данные УЗИ следует обязательно сопоставлять с данными анамнеза, клинической картиной, а также с результатами цитологического и радионуклидного исследований.
Огромное значение и важность цитологического метода в диагностике опухолей, в том числе и рака щитовидной железы, в настоящее время не вызывает сомнений. Главным принципом цитологической диагностики является определение клеточной формы опухоли, поскольку от этого зависит выбор оптимального метода лечения.
Метод очень прост в примененении. Для его выполнения необходим шприц с иглой и предметные стекла. Самым важным является здесь правильная интерпретация цитологических данных врачом-цитологом, что, несомненно, зависит от квалификации специалиста. Этот вид исследования позволяет качественно улучшить эффективность диагностики опухолей (чувствительность — 95,7%, специфичность — 82,3%, точность — 95,7%). Использование цитологического метода в ГУ РОНЦ им. Н.Н. Блохина РАМН позволило в 96% случаев правильно оценить первичный процесс в щитовидной железе, а в лимфатических узлах — в 93,4%. При этом в 78% возможно установить гистологическое строение опухоли (Т.Т. Кондратьева). При небольших размерах первичной опухоли и лимфатических узлов шеи тонкоигольная аспирационная биопсия под контролем УЗТ помогает повысить процент верификации при раке и регионарных метастазах.
Щитовидная железа из-за выраженной селективности захвата радиоактиактивного йода стала широко исследоваться методом радионуклидного сканирования. Поскольку 131I поглощается преимущественно нормальной тканью щитовидной железы, а поглощение радионуклида опухолевой тканью обычно ниже, то при подсчете импульсов над щитовидной железой в зоне опухолевых узлов отмечается меньшее накопление йода. Создается картина как бы дефектов накопления в щитовидной железе, которые в литературе и повседневной практике оцениваются как холодные узлы. С начала 60-х гг. ХХ в. появились публикации об использовании для сканирования технеция, который также селективно накапливается щитовидной железой, цитрата галлия, селенметионина, цезия.
Относительная ценность этого метода обусловлена тем, что некоторые доброкачественные образования щитовидной железы дают такую же картину. С другой стороны, опухоль небольших размеров, расположенная глубоко в ткани щитовидной железы, может не проявлять себя как холодный узел. Однако данные сканирования в сочетании с УЗИ, цитологическим исследованием позволяют в подавляющем большинстве случаев поставить правильный диагноз перед операцией.
Высока диагностическая ценность радиоизотопной диагностики в послеоперационном периоде, которая позволяет объективно оценить объем оставленных тканей щитовидной железы.
Артериография щитовидной железы с внедрением в практику КТ и МРТ потеряла свою диагностическую ценность, хотя на определенном этапе была высоко оценена для диагностики скрытого рака щитовидной железы (Кучинский Г.А., Пропп Р.М., 1973).
РКТ приобрела большое значение в диагностике различных опухолевых заболеваний за последние 25 лет. При диагностике рака щитовидной железы использование КТ преследует 2 цели:
1) попытка обнаружения маленького, скрыто протекающего рака щитовидной железы;
2) уточнение распространенности опухолевого процесса в отношении связи как первичного очага, так и регионарных метастазов в лимфатических узлах шеи и верхнего средостения с окружающими анатомическими образованиями (сосудами шеи, гортанью, трахеей).
Исследования, проведенные нами в последние годы у 65 больных раком щитовидной железы, показали, что применение РКТ в сочетании с МРТ позволяет в высоком проценте случаев до операции иметь информацию о взаимоотношении распространенной опухоли щитовидной железы с окружающими анатомическими структурами (рис. 3, 4, 5).
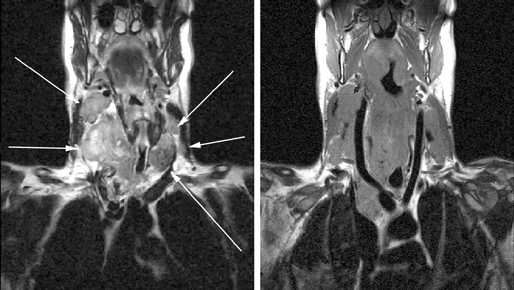
Рисунок 3. МРТ: опухолевое поражение обеих долей щитовидной железы, метастазы в лимфатические узлы шеи с обеих сторон и средостение
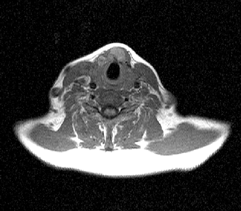
Рисунок 4. МРТ: опухолевое поражение перешейка щитовидной железы
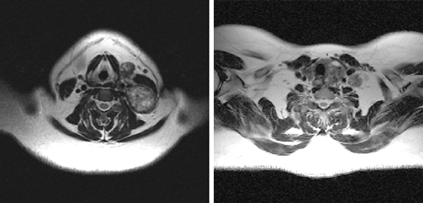
Рисунок 5. МРТ: опухолевое поражение нижнего полюса левой доли щитовидной железы
Многообразие форм злокачественных опухолей щитовидной железы, доброкачественных опухолей и опухолеподобных образований диктует необходимость дифференциальной диагностики этих новообразований. В первую очередь их следует дифференцировать от узлового зоба и аденомы. Для последних характерны более четкая и округлая форма, эластическая консистенция. Исчезновение сферичности контура железы или появление в ранее существующем зобе более плотных участков всегда должно вызывать подозрение на наличие рака.
Трудность дифференциальной диагностики узловых образований в щитовидной железе и начальной стадии рака предполагает более агрессивную тактику — хирургическое вмешательство на щитовидной железе. Объем операции при всех узловых образованиях должен заключаться в гемитиреоидэктомии с резекцией перешейка c обязательным последующим гистологическим исследованием. Указанная операция подобного объема служит как диагностическим, так и лечебным целям, поскольку она является адекватной для ранней стадии рака щитовидной железы.
Во время операции необходим тщательный осмотр удаленной опухоли. Хирург в большом проценте случаев может предположить наличие рака на основании макроскопического исследования. Рак щитовидной железы на разрезе чаще имеет гомогенное строение, напоминающее фиброму, бывает плотной консистенции. Цвет опухоли варьирует от белого до серовато-красного и бурого. Иногда на разрезе могут определяется очаги некроза. Вместе с тем при встречающейся чаще всего папиллярной аденокарциноме опухоль может напоминать строение зоба и содержать полости, наполненные жидкостью бурого цвета.
Необходимо также дифференцировать рак щитовидной железы от острых и хронических воспалительных процессов — тиреоидитов и струмитов специфического и неспецифического характера. Для острых тиреоидитов характерно равномерное увеличение щитовидной железы при сохранении ее контуров. Они протекают с повышением температуры тела, развиваются быстро и нередко связаны с каким-либо воспалительным процессом.
При тиреоидите де Кервена характерно увеличение всей щитовидной железы, неравномерная ее плотность, смещаемость, умеренное повышение температуры. При тиреоидите де Кервена относительно быстро в щитовидной железе появляются очаги размягчения.
Наконец, рак щитовидной железы следует дифференцировать от более часто встречающихся хронических тиреоидитов Хашимото и Риделя.
Для тиреоидита Хашимото характерен короткий анамнез (до года) у больных женщин, находящихся в пре— или климактерическом периоде, диффузное поражение щитовидной железы (в виде бабочки), явления гипотиреоза разной степени выраженности, плотноэластическая консистенция, без явлений перитиреоидита, умеренный лимфоцитоз в крови. В связи с аутоиммунной природой тиреоидита Хашимото при данном заболевании часто обнаруживается высокий титр циркулирующих антител против ТГ. В онкологическом центре с высокой точностью и достоверностью диагноз тиреоидита Хашимото ставится при пункции с последующим цитологическим исследованием.
По данным O. Clarc et al., больные с тиреоидитом Хашимото делятся на две группы:
1) с солитарными или преимущественно “холодными” узлами на сканограмме, при этом имеется относительно высокая (25%) степень риска развития злокачественной опухоли;
2) с диффузным увеличением щитовидной железы, при этом имеется очень низкий риск развития злокачественной опухоли. Эти больные могут лечиться консервативно.
Значительно труднее поставить правильный дооперационный диагноз при зобе Риделя. Заболевание чаще наблюдается у женщин, но в 30% случаев может встречаться и у мужчин. Анамнез также короткий. Поражается, как правило, одна доля. Узел в щитовидной железе плотной консистенции, быстро развиваются явления перитиреоидита и миозита шейных мышц, появляется ограничение смещаемости и рано наступает спаяние с трахеей, которое бывает достаточно интимным. Указанные признаки зоба Риделя обычно симулируют рак щитовидной железы. Поэтому всегда во всех сомнительных случаях показано цитологическое исследование либо биопсия.
Однако даже применение современных методов исследования в высококвалифицированных учреждениях не дает 100% точной дооперационной диагностики. Так, из 1121 пациента, лечившихся в нашей клинике за период с 1981 по 2000 г. при поступлении диагноз рак был установлен у 757 больных (67,5%), узловой зоб — у 176 (15,7%), аденома — у 160 (14,3%) и тиреоидит — у 18 (2,5%). Диагноз устанавливался на основании данных цитологического исследования и пересмотра готовых препаратов. Послеоперационное морфологическое исследование выявило рак щитовидной железы у 740 больных (66,1%), узловой зоб — 179 (16%), аденому — у 153 (13,6%) тиреоидит — 49 (4,3%) (Матякин Е.Г. и др., 2003). Приведенные данные показывают высокую степень совпадения дооперационного и послеоперационного диагноза с незначительной тенденцией к гипердиагностике рака в дооперационном периоде, что характерно для специализированного онкологического учреждения.
Лечебная тактика при раке щитовидной железы
Хирургическое лечение
Выбор лечебной тактики при раке щитовидной железы зависит от гистологического строения опухоли, распространенности процесса, пола, возраста больных, а также определяется некоторыми другими факторами. Ведущим в лечении рака щитовидной железы является хирургический метод. Если раньше онколог ставил перед собой задачу спасения больного, то сегодня надо думать и о функциональных последствиях в случае успешного завершения лечебных мероприятий.
Хирургическое лечение больных раком щитовидной железы представляет собой сложную задачу в связи с топографо-анатомическими особенностями расположения железы, высокой способностью опухоли к регионарному метастазированию, а также эндокринной функции данного органа.
Исходя из тактических соображений и онкологической настороженности, необходимо, как правило, отказаться от длительного консервативного лечения солитарно-узлового и многоузлового зоба. У таких больных, в том числе и детей, нужно проводить хирургическое вмешательство, поскольку надежным методом лечения у больных данной группы является своевременная операция.
До настоящего времени не утихают дискуссии в отношении объема оперативного вмешательства при раке щитовидной железы. Прежде всего необходимо указать на разноречивую, а часто и неправильную терминологию: тотальная, близкая к тотальной, субтотальная тиреоидэктомия, гемитиреоидэктомия и др. Необходимо определить четкие понятия, соответствующие характеру операции: гемитиреоидэктомия с резекцией перешейка, субтотальная резекция щитовидной железы и тиреоидэктомия. Такие объемы операции как энуклеация узла, энуклеация-резекция, резекция доли щитовидной железы не должны иметь место при узловом образовании щитовидной железы.
Дискутабельным остается вопрос об объеме операции при дифференцированном раке щитовидной железы. Основная причина этих споров — хорошие показатели выживаемости больных дифференцированным раком щитовидной железы. Большинство пациентов представлены так называемой группой низкого риска, где очень высокие показатели выживаемости.
Сложно согласиться со сторонниками рутинной послеоперационной терапии радиоактивным йодом в группе низкого риска. Выполнение тиреоидэктомии всем больным раком щитовидной железы влечет за собой высокую частоту специфических осложнений, а зачастую — инвалидность.
Национальный канцер-регистр США сообщил о 53865 наблюдениях рака щитовидной железы за период 1985—1995 гг. 10-летние показатели выживаемости для пациентов с папиллярным, фолликулярным, раком из клеток Ашкенази, медуллярным и недифференцированным (анапластическим) раком щитовидной железы составили 93, 85, 76, 75 и 14% соответственно. Соотношение гистологических форм рака щитовидной железы было следующим: папиллярный рак — 79,9%, фолликулярный — 14,2%, медуллярный — 3,7%, рак из клеток Ашкенази — 2,7% и недифференцированный рак — 1,6%. Согласно этой базе данных, показатели выживаемости при папиллярном и фолликулярном раках щитовидной железы не зависели от объема хирургического вмешательства.
Выделение групп риска дифференцированного рака щитовидной железы необходимо для выбора объема хирургического лечения. Подобное исследование проведено в США Клиникой Мейо, Клиникой Лехи, Чикагским университетом, Мемориальным центром рака Sloan—Kettering (Нью—Йорк). Наиболее важными прогностическими факторами в указанных исследованиях были следующие: возраст больных, гистологический вариант, наличие отдаленных метастазов, размер первичной опухоли, распространение за пределы железы. На основе этих факторов производится разделение больных на группы высокого и низкого риска с различными показателями выживаемости в группах.
Проведенные А.Р. Шаха (2003) исследования в мемориальном центре рака Sloan—Kettering позволяют делить прогностические факторы на связанные с пациентом и связанные с опухолью. Пациенты были разделены на группы низкого, промежуточного и высокого риска. Группа низкого риска состояла из пациентов низкого риска (возраст моложе 45 лет) с опухолями низкого риска. Группа высокого риска состояла из пациентов высокого риска (старше 45 лет) с опухолями высокого риска. Группа промежуточного риска состояла из двух категорий: пациенты низкого риска с опухолями высокого риска и пациенты высокого риска с опухолями низкого риска. Показатели выживаемости составили 99% в группе низкого риска, 87% — в группе промежуточного риска и 57% — в группе высокого риска. Таким образом, приведенные данные показывают, что выбор объема хирургического вмешательства должна определять группа риска. В группе низкого риска, где лечение радиоактивным йодом не показано, адекватной операцией может быть гемитиреоидэктомия с резекцией перешейка либо субтотальная резекция щитовидной железы. В группе высокого риска, учитывая необходимость дальнейшей терапии радиоактивным йодом, необходим агрессивный хирургический подход. В группе промежуточного риска решение вопроса об объеме вмешательства должно базироваться, главным образом, на связанных с опухолью факторах. Например, для опухоли высокого риска, где может понадобиться послеоперационное лечение радиоактивным йодом, адекватным объемом операции является тиреоидэктомия. Низкая степень дифференцировки опухоли определяет высокий риск развития местного рецидива, необходимость терапии радиоактивным йодом и наружное облучение (многие низкодифференцированные опухоли плохо захватывают радиоактивный йод).
Сторонники рутинной тиреоидэктомии аргументируют подобный подход частым наличием микроскопических очагов рака в противоположной доле щитовидной железы, частой необходимостью лечения радиоактивным йодом, необходимостью послеоперационного наблюдения с помощью сканирования тела или определения уровня ТГ, что затруднительно при наличии остаточной ткани щитовидной железы. Среди аргументов называют также вероятность анапластической трансформации тиреоидного остатка и возможность отдаленного метастазирования.
Указанные аргументы недостаточно обоснованы в группе низкого риска с выживаемостью 99%. Сторонники агрессивного подхода считают, что тиреоидэктомия снижает число рецидивов и улучшает показатели выживаемости. Ввиду отсутствия кооперированного международного исследования эти вопросы остаются дискутабельными.
На сегодняшний день не вызывает сомнения необходимость тиреоидэктомии у пациентов высокого риска с опухолями высокого риска. В эту группу включаются:
— молодые пациенты с большими первичными опухолями и массивным поражением лимфатических узлов, что предполагает лечение радиоактивным йодом;
— пациенты с поражением обеих долей щитовидной железы;
— пациенты с экстратиреоидным распространением опухоли;
— пациенты с выявленным до операции низкодифференцированным раком;
— пациенты с медуллярной аденокарциномой щитовидной железы;
— пациенты с раком щитовидной железы при наличии облучения в анамнезе;
— пациенты с резектабельной анапластической аденокарциномой;
— пациенты с наличием отдаленных метастазов.
Объем хирургического вмешательства при медуллярном раке щитовидной железы отличается от такового при дифференцированных формах рака. Медуллярный рак щитовидной железы — аутосомно-доминантное семейное заболевание, которое может протекать в спорадической или наследственной форме, включая синдромы МЭН I и II типов. В отношении медуллярного рака общепринятым является агрессивный хирургический подход — тиреоидэктомия с центральной диссекцией во всех случаях. Профилактическая модифицированная шейная лимфодиссекция, как правило, не производится.
Однако в последние годы появились работы (Бржезовский В.Ж. и др., 2003 г.; Романчишен А.Ф. и др., 2003), в которых авторы после более экономных вмешательств у 22 больных медуллярным раком щитовидной железы с опухолью размером до 2 см производили гемитиреоидэктомию с перешейком. Рецидив рака в дальнейшем не выявлен. Причиной смерти в течение последних 5 лет у 3 больных (13,6%) явилась генерализация опухолевого процесса (метастазирование рака в легкие и кости).
При размерах опухоли от 2 до 4 см 46 больным была выполнена субтотальная резекция щитовидной железы. При гистологическом исследовании в 5 случаях выявлено прорастание капсулы щитовидной железы. При последующем наблюдении в сроки до 5 лет рецидив в оставшейся доле щитовидной железы выявлен у 4 пациентов (8,7%). Наш более скромный опыт, включающий около 30 больных медуллярным раком щитовидной железы, позволяет говорить о том, что подавляющее большинство пациентов медуллярным раком щитовидной железы поступили с распространенными процессами. Ограниченное поражение встретилось в единичных случаях, и было гистологически выявлено после операции по поводу предполагавшихся других форм опухоли щитовидной железы. Поэтому мы, как и большинство других авторов, настаиваем на расширенном объеме вмешательства при медуллярном раке щитовидной железы.
Анапластический рак щитовидной железы является одной из наиболее агрессивных опухолей человека. В большинстве наблюдений это заболевание является фатальным. Средняя продолжительность жизни в этой группе больных составляет 6–9 мес. При этом быстро вовлекаются в процесс дыхательные пути, появляются метастазы в легких. Полное удаление опухоли возможно лишь у 20% пациентов. Однако в некоторых случаях при небольшой опухоли возможна тиреоидэктомия. Нередко операция сводится к декомпрессии трахеи и наложению трахеостомы.
Нет единства мнений в отношении объема операции и при микрокарциноме щитовидной железы. Однако высокая вероятность мультицентрического роста с поражением в обеих долях позволяет рекомендовать операцию в объеме тиреоидэктомии.
Операции на щитовидной железе при раке выполняются с учетом двух принципиальных положений: они должны быть онкологически радикальными и эндокринологически адекватными. При операции необходима широкая ревизия всей щитовидной железы и зон регионарного метастазирования, оценка операционных находок и выбор объема вмешательства в зависимости от указанных факторов. Операции по поводу рака следует проводить экстракапсулярно. Важно иметь широкий доступ для ревизии операционного поля. Для этого необходимо широко отсепаровывать кожно-жировые лоскуты и обязательно пересекать передние длинные мышцы шеи (при инфильтрации мышц опухолью последние резецируются). Затем отсепаровывают грудино-ключично-сосцевидные мышцы и отводят их в стороны.
Для предупреждения возможного распространения опухолевых элементов целесообразно на I этапе перевязать верхние и нижние щитовидные артерии. Нижняя щитовидная артерия, из-за интимного расположения рядом с возвратным нервом, перевязывается после его выделения. Выделение возвратных нервов является обязательным при всех трех типах операций на щитовидной железе. Следует отметить, что этот нерв очень чувствителен к ранениям, и даже легкая травматизация может привести к парезу или параличу голосовых складок.
Верхний гортанный нерв имеет смешанную природу. Наружная его ветвь проходит рядом с верхней щитовидной артерией. При высоком расположении верхнего полюса щитовидной железы и перевязке верхней щитовидной артерии возможна его травма, ведущая к потере чувствительности в области надгортанника. При этом больной хорошо глотает твердую пищу, а жидкая пища попадает “не в то горло”.
К.Р. Цернеа и соавт. (2003), изучавшие прикладную анатомию верхнего гортанного нерва, говорят о том, что повреждение верхнего гортанного нерва вызывает паралич перстне-щитовидной мышцы, нарушая высокие тона голоса, что является серьезным осложнением, особенно для женщин и профессиональных певцов. Поэтому важным техническим аспектом является профилактика повреждения нерва путем расширения знаний анатомических вариантов в области верхнего полюса щитовидной железы, а также тщательное выделение и бережное обращение с верхней щитовидной артерией.
При операции необходимо идентифицировать и сохранить паращитовидные железы. Иногда тетания может развиться и при сохранности этих желез. Обусловлено это перевязкой и пересечением проходящих в капсуле щитовидной железы артериальных веточек, питающих паращитовидные железы.
Во время операции необходим гемостаз, особенно в области вхождения возвратного нерва в гортань. Трахея ротируется, и лучше видны небольшие сосуды, кровотечение из которых останавливается путем прижатия тампона.
Вопросы о целесообразности операции при распространенных формах рака щитовидной железы до сих пор дискутируются. А.Ф. Романчишен и соавт. (2003), имеющие опыт лечения 280 таких больных считают, что о местно-распространенных формах рака говорить следует либо в случае инвазии опухоли в близлежащие ткани, либо при обширном регионарном метастазировании. Наиболее часто местно-распространенные формы рака щитовидной железы наблюдались у больных в возрасте 50—60 лет. Гистологически преобладают высокодифференцированные формы. Обширное регионарное метастазирование выявлено у 137 (49,9%), отдаленные метастазы — у 38 (32,5%). Из указанного числа больных расширенные операции произведены 38 (13,5%). Комбинированные — 72 (23,7%), паллиативные — 133 (43,8%). В 18 наблюдениях произведена стернотомия с целью выполнения медиастинальной лимфаденэктомии.
В ряде случаев наряду с тиреоидэктомией приходится резецировать от 5 до 9 колец трахеи, выполнять ларингэктомию, нередко с резекцией гортаноглотки.
Паллиативные операции выполняются, как правило, при недифференцированном раке (52,4% случаев).
Наиболее эффективным методом лечения регионарных метастазов является хирургическое вмешательство. Касаясь операции на лимфатических коллатералях шеи и средостении, нельзя не коснуться таких понятий как зональность и футлярность.
Анатомическая зональность — это пути и этапы местного лимфатического метастазирования. В это понятие вкладывается представление о строго определенной анатомической территории тканей, подлежащих удалению. Понятие анатомической футлярности исходит из данных о футлярном строении отдельных зон человеческого тела. Каждый орган или анатомическая часть отделены друг от друга фасциальными, плевральными, брюшинными или жировыми прослойками, создающими подобие футляра, замкнутого со всех или нескольких сторон. Удаление опухоли в пределах такого футляра является наиболее абластичным (принцип футлярности).
В настоящее время при удалении регионарных метастазов на шее используются 2 варианта вмешательств:
1) операция Крайла, предложенная автором в 1906 году;
2) фасциально-футлярное иссечение клетчатки шеи, разработанное в конце 60-х гг. ХХ в. в ГУ РОНЦ им. Н.Н. Блохина.
Обе операции имеют строгие показания к выполнению.
Операция Крайла
Производится при метастазах, спаянных с анатомическими образованиями шеи (внутренней яремной веной, грудино-ключично-сосцевидной мышцей, добавочным и блуждающим нервами). При этой операции помимо удаления клетчатки и лимфатических узлов шеи, производится резекция грудино-ключично-сосцевидной мышцы, внутренней яремной вены, добавочного нерва и, в классическом варианте, заднего брюшка двубрюшной и шило-подъязычной мышц. Иногда при распространенном метастатическом поражении резецируется блуждающий нерв, симпатический шейный ствол и лестничные мышцы с покрывающей их 5 фасцией шеи, наружная сонная артерия.
Фасциально-футлярное иссечение клетчатки шеи
Это более функциональная операция, при которой сохраняются все вышеуказанные анатомические образования шеи. Выполняется на лимфатических узлах, не спаянных с анатомическими образованиями шеи, а также при т.н. превентивных операциях, т.е. в случаях, когда лимфатические узлы шеи не пальпируются.
Вопрос о целесообразности использования превентивных операций при раке щитовидной железы, особенно дифференцированных его формах, до настоящего времени не решен.
Ш. Ногучи (2003), имеющий опыт выполнения модифицированных шейных диссекций (вариант фасциально-футлярного иссечения клетчатки шеи) сообщил: из 2210 пациентов с папиллярным раком щитовидной железы у 1160 (52,5%) до операции клинически и макроскопически регионарные метастазы не определялись. Из числа последних у 984 (84,8%) после гистологического исследования выявлены регионарные метастазы. Из 264 наблюдений выполнения центральной лимфодиссекции в 46 (17,2%) случаях были обнаружены метастазы в лимфатических узлах. На основании собственного опыта хирург считает необходимым выполнение превентивных операций при высокодифференцированных аденокарциномах щитовидной железы. Вместе с тем автор утверждает, что наличие явных метастазов определенно оказывает влияние на выживаемость лишь у больных пожилого возраста. На основании многолетнего наблюдения за больными он делает вывод: наличие явных метастазов в лимфатических узлах в момент диагностики является одним из прогностических факторов при папиллярном раке щитовидной железы. Однако среди пациентов без определяемых метастазов, микрометастазы обнаруживаются почти в 80% случаев. Эти метастазы обычно не значимы для прогноза, однако наличие этих мелких метастазов может впоследствии приводить к неблагоприятному исходу.
Большинство других авторов, занимающихся лечением рака щитовидной железы, более решительно выступают против превентивных операций на шее при высокодифференцированных аденокарциномах щитовидной железы. Что касается выполнения этих операций при медуллярном и низкодифференцированном раке, проблема не встает столь же остро, так как процент регионарных метастазов при этих формах значительно высок при поступлении, и радикальные операции на шее выполняются чаще всего с лечебной целью. При недифференцированном раке, кроме того, основной проблемой является возможность удаления первичной опухоли.
При фасциально-футлярном иссечении клетчатки шеи разрез производится от сосцевидного отростка и далее идет вниз по заднему краю грудино-ключично-сосцевидной мышцы. В надключичной области он продолжается по нижней шейной складке до переднего края грудино-ключично-сосцевидной мышцы с противоположной стороны. Кожные лоскуты отсепаровываются в стороны и грудино-ключично-сосцевидная мышца отводится кнаружи. После операции на щитовидной железе производится удаление клетчатки и лимфатических узлов надключичной области, бокового треугольника шеи, лимфатических узлов и клетчатки вдоль глубокой яремной вены, а также клетчатки акцессорной области. Клетчатка и лимфатические узлы подчелюстной и подбородочной областей не удаляются, так как метастазы рака щитовидной железы в этих зонах реализуются крайне редко. Одномоментно с удалением первичного очага удаляется клетчатка и лимфатические узлы паратрахеальной и претрахеальной зон, а также преларингеальные узлы.
При метастазах в области передневерхнего средостения часто имеется возможность мобилизовать эти узлы через яремную вырезку грудины. Однако при обширном поражении лимфатических узлов средостения необходимо производить стернотомию, чтобы абластично удалить всю клетчатку и метастазы переднего, а иногда и заднего средостения.
Обладая большим опытом таких операций и принимая во внимание, что публикации по технике данной операции крайне редки и изложены достаточно кратко, осветим эту проблему несколько подробнее. Данные по лечению опухолей верхней грудной апертуры были нами доложены на Российском симпозиуме с международным участием в июле 2003 г. (Давыдов М.И. и соавт., 2003).
Всего за период с 1991 г. по настоящее время нами оперировано 34 больных с опухолями щитовидной железы. У 32 из них имелся первичный очаг или регионарные метастазы рака щитовидной железы. Из них у 28 выявлен папиллярный рак щитовидной железы, у 3 — медуллярный и в одном случае — недифференцированный. Двое пациентов оперированы по поводу внутригрудного зоба.
Оперативные вмешательства в такой ситуации носят комбинированный характер и выполняются как на шее, так и в средостении. В зависимости от распространенности и локализации процесса имеется несколько вариантов последовательности выполнения оперативного вмешательства.
Первый вариант
При аденокарциномах щитовидной железы, чаще всего имеющих метастазы не только в лимфатические узлы средостения, но и поражающих лимфатический аппарат шеи, операция начинается со стернотомии. На передней поверхности шеи производится разрез по нижней шейной складке (типа Кохера) и от него выполняется разрез вниз по грудине, который поворачивается на уровне 4—5 межреберья, чаще влево, если производится косая стернотомия. В случае срединной стернотомии разрез кожи проводится до мечевидного отростка. После стернотомии и разведения в стороны фрагментов грудины производится удаление клетчатки и метастатических узлов средостения от уровня дуги аорты. Операция заканчивается радикальным вмешательством на шее с одной или с двух сторон и тиреоидэктомией.
Второй вариант
В случае поражения трахеи, после стернотомии производится резекция колец трахеи с одномоментной пластикой. При поражении гортани одновременно с резекцией верхних колец трахеи выполняется ларингэктомия. Глотка ушивается, оформляется постоянная трахеостома. Препарат в данном случае удаляется в едином блоке со щитовидной железой, клетчаткой и лимфоузлами средостения. При необходимости выполняется радикальная операция на шее с одной или с двух сторон.
Третий вариант
При изолированном поражении метастазами лимфатических узлов средостения, внутригрудном зобе разрез кожи производится, как и в первом варианте. Выполняется удаление зоба или лимфодиссекция. На шее операция ограничивается вмешательством только в нижних отделах передней ее поверхности.
Первый вариант операции выполнен у 22 пациентов. При этом у 2 больных произведена резекция легкого, у 2 — удалены метастазы в заднем средостении, у одного больного удален атипично расположенный узел, локализовавшийся под лестничными мышцами шеи. Радикальные операции на шее выполнены у 12 пациентов. У 8 пациентов, наряду с поражением узлов средостения, имелись множественные метастазы в легкие. После выполнения операции они направлены на лечение радиоактивным йодом. Второй вариант операции выполнен у 4 пациентов, третий — у 6. Еще у двух больных анатомическое строение нижних отделов шеи и передне-верхнего средостения было таково, что удалось вывести на шею плечеголовной ствол аорты, и клетчатка с метастатическими узлами этой зоны удалена через шею. При наблюдении от нескольких месяцев до 12 лет живы 25 пациентов (73,5%). Опыт выполнения таких операций позволяет рекомендовать их применение в лечебной практике.
Хирургические вмешательства при рецидивах и после нерадикальных операций имеют свои особенности. Мы ранее говорили о том, что опухолевое поражение при рецидивах, как правило, бывает более распространенным, чем при первичной опухоли. Кроме того, значительные трудности при операции обусловлены выраженными рубцовыми изменениями в окружающих тканях. Эта касается и операций, выполняемых после нерадикальных вмешательств. Н.С. Кузнецов с соавт. (2003) при выполнении повторных вмешательств в объеме тиреоидэктомии выявили, что более чем у половины больных с первичными опухолями диаметром около 1 см, имеются очаги рака в контралатеральной доле щитовидной железы.
Если у больного после нерадикальной операции есть уплотнение в области операционного рубца или наступает очевидный рецидив рака щитовидной железы, либо появляются регионарные метастазы, необходимость лечения очевидна. А что делать с больными, у которых после экономных операций нет проявлений болезни? Опыт показывает, что потребность в повторных операциях необходима. Данные Н.С. Кузнецова с соавт. (2003) подтверждают это положение. Многолетний опыт лечения таких больных свидетельствует: всем больным после экономных операций на щитовидной железе необходимо выполнять радиоизотопное исследование. В большинстве случаев, даже если в выписке указано, что произведена субтотальная резекция щитовидной железы, либо гемитиреоидэктомия, при радиоизотопном исследовании отмечается накопление РФП в якобы удаленных тканях. В этих случаях вмешательство необходимо.
Особенностью оперативного вмешательства при рецидивах рака щитовидной железы и после экономных операций является необходимость обязательного включение в блок удаляемых тканей передних длинных мышц шеи, т.к. велика вероятность поражения опухолевым процессом указанных образований. Кроме того, совершенно необходимо выполнять, так называемую, переднюю шейную диссекцию — удаление паратрахеальной, претрахеальной и преларингеальной клетчатки вместе с находящимися в ней лимфатическими узлами. Эта тактика обусловлена тем, что при повторных операциях вероятность реализации регионарных метастазов в этой зоне увеличивается.
Дополнительные методы лечения
Дистанционная лучевая терапия
Дистанционная лучевая терапия для комплексного лечения дифференцированных форм рака щитовидной железы применяется крайне редко. В нескольких исследованиях показано, что применение лучевой терапии в комплексе с тотальной тиреоидэктомией, радиойодаблацией и супрессией тиреотропного гормона (ТТГ) — улучшает безрецидивную выживаемость в группе пациентов старше 45 лет с инвазивным папиллярным раком щитовидной железы при первичной опухоли Т4 и регионарными метастазами, соответствующими символу N1. При использовании лучевой терапии у больных с резидуальным папиллярным раком выживаемость без рецидива повысилась с 26 до 90%, а при фолликулярном раке с 38 до 53%. Другие авторы сообщают, что применение лучевой терапии не влияет на летальность. Что касается предоперационной лучевой терапии, то мы не являемся ее сторонниками. Мы считаем неоправданным назначение предоперационного облучения при медленно растущем дифференцированном раке щитовидной железы, даже с наличием регионарных метастазов, когда в полном объеме возможно адекватное хирургическое вмешательство.
Супрессивная терапия левотироксином натрия
По сообщениям многих исследователей, показатели летальности уменьшаются при использовании супрессивной терапии левотироксином натрия с подавлением ТТГ сыворотки крови. В отличие от заместительной терапии с нормальными значениями ТТГ, (средняя дозировка левотироксина натрия в данном случае составляет 1,6—1,7 мкг/кг/сут) при супрессивной терапии доза левотироксина натрия составляет 2,0—2,5 мкг/кг/сут. Однако нормальный уровень ТТГ крови, который необходимо достигать при супрессивной терапии, остается спорным.
Радиойодаблация
Необходимым условием применения радиоактивного йода (131I) при отдаленных метастазах рака щитовидной железы является выключение железы, как фактора, стимулирующего йодконцентрирующую способность метастазов. Применение радиоактивного йода также необходимо у всех пациентов с потенциально возможным рецидивом опухоли. Многие исследователи отмечают снижение числа рецидивов и летальности в группе больных, где на начальном этапе лечения была применена радиойодтерапия. В исследовании, сравнивающем результаты лечения 1004 больных с дифференцированным раком щитовидной железы, рецидив опухоли был достоверно ниже в группе пациентов, где была применена послеоперационная радиойодтерапия, по отношению к группе пациентов, находящихся только на супрессивных дозах заместительной терапии. Кроме того, в группе, где была проведена терапия радиоактивным йодом, отмечено снижение числа отдаленных метастазов по сравнению с группами пациентов, подвергавшихся другим методам послеоперационного лечения (подобные результаты наблюдались только при опухолях менее 1,5 см в диаметре).
Выделены три основные причины необходимости проведения радиойодтерапии:
1. С практической точки зрения не представляется возможным полностью удалить щитовидную железу. Этот факт подтвержден результатами сцинтиграфии с радиоактивным йодом, который практически всегда накапливается в ложе удаленной щитовидной железы. Уничтожение остаточной тиреоидной ткани необходимо для максимальной концентрации радиоактивного йода в возможных метастазах в регионарные лимфатические узлы и легкие.
2. Максимальные значения ТТГ крови, необходимые для проведения радиойодтерапии (увеличивается поглощение 131I опухолью) не могут быть достигнуты при оставшейся тиреоидной ткани, особенно после гемитиреоидэктомии.
3. Аблация необходима для послеоперационного наблюдения за пациентами с изучением уровня сывороточного ТГ крови на фоне максимальной стимуляции ТТГ, что в принципе не реализуется при сохранении даже минимального количества тиреоидной ткани.
Что касается дозировки радиоактивного йода, то и в этом вопросе нет единого мнения. Е.С. Киселева и Р.Л. Седракян (1975) показали эффективность лечения разовыми активностями в 50—100 мкКи с интервалом 2—3 мес. Суммарные активности составили 715 мкКи. В настоящее время большинство зарубежных авторов применяют более высокие терапевтические разовые активности — 100—250 мкКи и всего 3—5 таких доз с перерывами в несколько месяцев. Между курсами лечения проводят заместительную терапию тиреоидными гормонами, которую прекращают за 3 нед до начала лечения.
Заключая раздел по применению радиойодтерапии, следует отметить, что последняя позволяет завершить тиреоидэктомию на клеточном уровне, уменьшить вероятность рецидива опухоли, создать условия для ранней диагностики и лечения отдаленных метастазов, обеспечить возможность дальнейшего наблюдения за больными по уровню ТГ в сыворотке крови.
Лекарственное лечение
Рак щитовидной железы относится к категории новообразований, на которые противоопухолевые препараты оказывают незначительное терапевтическое воздействие, либо не оказывают воздействия вообще. По сводным данным литературы, положительная реакция рака щитовидной железы на различные лекарственные препараты ограничена в пределах 10—15%. Наиболее эффективными оказываются схемы лечения, включающие доксорубицин, фторурацил, препараты платины (табл. 2).
Таблица 2
Схемы лечения рака щитовидной железы
| Комбинация | Лекарственные средства, доза и режим лечения |
| Папиллярный рак щитовидной железы | |
| AB | Доксорубицин — по 50-60 мг/м2, в/в, в 1 день, Блеомицин — по 30 мг, в/в, в 1-3 дни |
| Доксорубицин — по 70 мг/м2, в/в, в 1 день, Винкристин — по 1,4 мг/м2 в 1 и 8 дни, Блеомицин — по 15 мг, в/в, в 1-5 дни. Циклы повторяют с интервалом в 3 нед |
|
| Медуллярный рак щитовидной железы | |
| CAP | Циклофосфамид — по 750 мг/м2, в/в, в 10 день, Доксорубицин — по 50 мг/м2 в 1 день, Цисплатин — по 20 мг/м2, в/в, в 1-5 дни. Циклы повторяют с интервалом в 3 нед |
| PABP | Цисплатин — по 100 мг/м2, в/в, в 4 день, Доксорубицин — по 60 мг/м2, в/в, в 1 день, Блеомицин — по 15 мг, в/в, в 1-4 дни, Преднизолон — по 1 мг/кг внутрь в 1-5 дни |
При недифференцированных раках щитовидной железы в различных комбинациях используются следующие препараты: доксорубицин, циклофосфамид, ифосфамид, цисплатин.
Чаще всего эти и другие препараты применяются после паллиативной операции, а также при анапластических формах рака. Шаха и соавт. (2003) сообщают, что в случае гигантоклеточного варианта анапластического рака щитовидной железы основное значение имеет сочетание химиотерапии и наружного облучения. На сегодняшний день обнадеживают результаты применения паклитаксела в сочетании с гиперфракционированной лучевой терапией. Вопросы химиолучевого лечения рака щитовидной железы должны стать предметом дальнейшего изучения.
Результаты лечения
Касаясь различных форм рака щитовидной железы, мы уже писали о факторах, влияющих на появление рецидива первичной опухоли, реализации регионарных метастазов, выживаемости, поэтому в этом разделе коснемся лишь обобщающих работ, посвященных данному вопросу.
Международная классификация рTNM в достаточной степени позволяет прогнозировать причинно-специфическую летальность при папиллярном раке щитовидной железы. Через 10 лет после операции для стадии I, II, III и IV летальность составила 0,4; 2,3; 12 и 88,4% соответственно по данным I.D. Hay (1990). Если объединить стадии I и II в группу низкого риска, a стадии III и IV — в группу высокого риска, то 20-летняя летальность для групп низкого и высокого риска окажется 1,35 и 24,8% соответственно, с соотношением (большего к меньшему) 19:1. Прогностическая система AGES, основанная на показателях возраста (Age), гистологических характеристиках (Grade), распространенности (Extent) и размерах первичного очага (Size) делит больных папиллярным раком щитовидной железы на группу низкого риска, с показателями менее 4, и группу высокого риска, с показателями более 4. Через 20 лет, при оценке групп риска по AGES, летальность для группы низкого и высокого риска оказалась 1,0 и 36,4% соответственно, с соотношением уровней летальности 1:36 (Hai J.D. et al., 1987).
Схема AMES, предложенная B. Cady (1988), основанная на критериях возраста (Age), метастазов (Metastasis), экстратиреоидной инвазии (Extra thyroid invasion) и размеров первичного очага (Size) подразделяет пациентов на группы низкого риска с летальностью через 20 лет, равной 1,1%, и группу высокого риска с показателем 38,8%; соотношение между группами 1:35.
Прогностическая схема, предложенная I.D. Hay et al. (1999), разработанная путем анализа по методу COX и постепенно меняющейся селекции признаков, которая из 1779 больных папиллярным раком щитовидной железы, прослеженных суммарно более 26 тыс. человеколет, была названа MACIS и включала в себя критерии наличия метастазов (Metastasis), возраст (Age), полноту удаления первичной опухоли (Completeness of initial tumor resection) и размер опухоли — максимальный диаметр (Size of tumor maximum diameter). Через 20 лет в группе больных низкого риска с показателем менее 6, мы получили удовлетворительный показатель летальности — 0,8%, в то время как в группе высокого риска 20-летний уровень летальности составил 31,9% с соотношением 1:40.
Для 2099 пациентов группы низкого риска (по шкале MACIS менее 6) показатель летальности через 25, 30 и 40 лет оказался равным 0,9; 1,7 и 2,3% соответственно. А при сравнении с группой высокого риска из 413 пациентов (по шкале MACIS более 6) показатель составил 34,6; 37 и 37% соответственно.
Фолликулярная аденокарцинома обладает бóльшей склонностью к отдаленному метастазированию, чем папиллярный рак. Так, по данным Н.С. Кузнецова с соавт. (2003), до 25% больных фолликулярным раком щитовидной железы имеют отдаленные метастазы. Вместе с тем другими авторами приводятся более высокие цифры 5— и 10-летней безрецидивной выживаемости. Так, по данным А.И. Пачес и Р.М. Пропп (1995), 5— и 10-летняя выживаемость при папиллярной аденокарциноме — 95,3 и 94,2% соответственно, при фолликулярной аденокарциноме — 90,1 и 85,7%; а при медуллярном раке — в 87, 2 и 80% соответственно.
Медуллярный рак щитовидной железы встречается относительно редко (3—10% всех случаев рака этого органа) поэтому большинство клиник не имеют достаточного опыта в лечении данного заболевания и, следовательно, отсутствуют обобщающие данные по прогнозу этого вида новообразования, подобно тому, какие имеются при папиллярной аденокарциноме. Вместе с тем на основании опыта лечения 83 больных медуллярным раком щитовидной железы А.Ф. Романчишен с соавт. (2003) приводят данные о том, что 5-летняя выживаемость всех больных составила 78,8%. Неблагоприятный прогноз определяли выход опухоли за пределы железы, распространение опухоли на лимфатические узлы средостения, наличие регионарных метастазов. В группе больных, перенесших органосохраняющие операции (при ограниченных процессах), 5-летняя выживаемость составила 89,4%, после тиреоидэктомии (при III и IV стадиях) — 51,4%. Причиной смерти больных были отдаленные метастазы и массивное поражение регионарных лимфатических узлов. В.Ж. Бржезовский и соавт. (2003) говорят о том, что из 68 больных с размером опухоли до 4 см, которым выполнены органосохраняющие операции, умерло 20 пациентов (29,4%). Только у 3 из них (4,4%) выявлены рецидивы первичной опухоли. Смерть больных наступала от генерализации опухолевого процесса.
При анапластическом раке прогноз зависит только от местного распространения опухоли. По данным А.И. Пачес, Р.М. Пропп (1995) при этой форме рака никто из наблюдавшихся больных не прожил более 5 лет. Большинство авторов считают: если больной с анапластическим раком живет больше года, следует пересмотреть диагноз. Несмотря на то, что с этим утверждением согласиться трудно, думается: приводимые некоторыми авторами показатели выживаемости у больных с недифференцированным раком щитовидной железы (5-летняя выживаемость от 2 до 29,6%), безусловно, завышены. Это можно объяснить трудностями морфологической диагностики. А также тем, что у многих авторов материал собран за долгие годы и не пересмотрен. Поэтому, вероятно, в группу недифференцированного рака вошел и медуллярный рак.
При диагностическом наблюдении за больными каждые полгода необходимо выполнять следующие исследования:
— рентгенография грудной клетки,
— анализ крови,
— определение уровня тиреоидных гормонов,
— УЗИ шеи,
— сканирование щитовидной железы в первый год после операции.
Особенности биологического и клинического течения рака щитовидной железы и оптимальные лечебная тактика и техника хирургического вмешательства позволяют добиться хороших ближайших и отдаленных результатов.
Описание проверено экспертом
Оцените статью:
- Рак щитовидной железы
- Карцинома щитовидной железы
- Тиреотропинзависимые карциномы щитовидной железы
- Анапластический рак щитовидной железы
- Медуллярный рак щитовидной железы
- Опухоли щитовидной железы
- Папиллярный рак щитовидной железы
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).
злокачественное новообразование щитовидной железы
перед или во время применения радиоактивного йода для лечения карциномы щитовидной железы или сцинтиграфии, рак щитовидной железы, при подозрении на рак щитовидной железы, наличием метастазов рака щитовидной железы в органах,


