I42.1 Обструктивная гипертрофическая кардиомиопатия, МКБ-10
Отредактировано: 05.07.2024
Гипертрофическая кардиомиопатия
Определение и классификация
Гипертрофическая кардиомиопатия (ГКМП) – генетически детерминированное заболевание, проявляющееся массивной гипертрофией миокарда преимущественно левого желудочка и приводящее к уменьшению его полости, развитию диастолической дисфункции и нередко – к обструкции выносящего тракта левого желудочка (ВТЛЖ).
В повседневной клинической практике используют несколько классификаций ГКМП [1]:
Гемодинамическая классификация
В зависимости от наличия или отсутствия обструкции ВТЛЖ в покое и при нагрузке выделяют следующие варианты ГКМП:
- Необструктивная ГКМП (градиент давления в ВТЛЖ <30 мм рт. ст. в покое и при нагрузке);
- Обструктивная ГКМП (градиент давления в ВТЛЖ >30 мм рт. ст. в покое и при нагрузке);
- Латентная обструкция (градиент давления в ВТЛЖ <30 мм рт. ст. в покое и >30 мм рт. ст. при нагрузке).
Морфологическая классификация
1. Асимметричная форма ГКМП.
1.1. Гипертрофия межжелудочковой перегородки (с или без вовлечения правого желудочка):
- Гипертрофия базальной части межжелудочковой перегородки (субаортальная);
- Сигмовидная межжелудочковая перегородка;
- Гипертрофия всей межжелудочковой перегородки;
- Двояковыпуклая межжелудочковая перегородка (англ. «reverse curve», преимущественно среднежелудочковая гипертрофия межжелудочковой перегородки без вовлечения свободной стенки левого желудочка) [2, 3];
- Комбинированная гипертрофия (гипертрофия межжелудочковой перегородки с вовлечением другого отдела левого или правого желудочка).
1.2. Апикальная гипертрофия (с или без вовлечения срединных сегментов левого желудочка.
1.3. Среднежелудочковая ГКМП (с вовлечением срединных отделов не только межжелудочковой перегородки, но и свободной стенки левого желудочка, левый желудочек типа «песочные часы»).
1.4. Гипертрофия другой стенки левого желудочка (боковая, задняя).
2. Симметричная форма ГКМП.
В литературе иногда используется термин «диффузная гипертрофия левого желудочка», под которым понимают комбинированную или симметричную ГКМП [4].
Клиническая классификация
Выделяют следующие клинические варианты течения ГКМП:
- Дебют болезни в виде внезапной сердечной смерти* (ВСС);
- Бессимптомное течение;
- Симптомное стабильное (на фоне медикаментозной терапии) доброкачественное течение;
- Симптомное осложненное течение (развитие хронической сердечной недостаточности, фибрилляции предсердий, стенокардии);
- Симптомное течение с негативным ремоделированием левого желудочка (прогрессирование явлений хронической сердечной недостаточности или формирование апикальной аневризмы левого желудочка).
Этиология и патогенез
ГКМП – это генетически обусловленная патология, наследуемая по аутосомно-доминантному типу с неполной пенетрантностью. В основе развития ГКМП чаще всего лежат мутации в генах, кодирующих сократительные белки саркомера – миозин (MYH7), миозинсвязывающий белок С (MYBPC3), актин (ACTC), тропонин (TNNI3, TNNT2, TNNC) [5].
Отдельно принято выделять фенокопии ГКМП – заболевания генетической и негенетической природы, по морфофункциональному фенотипу схожие с ГКМП, но имеющие отличный от нее этиопатогенез и, следовательно, подходы к терапии. К ним относятся:
- Амилоидоз;
- Болезнь Андерсона-Фабри;
- Наследственные синдромы, связанные с мутациями в гене PRKAG2;
- Болезнь Данона;
- Атаксия Фридрейха;
- RASопатии (синдром Нунан и LEOPARD).
В основе молекулярного патогенеза ГКМП часто лежит нарушение кальциевого гомеостаза и повышение чувствительности миофиламентов к ионам кальция [6]. В результате увеличивается сила сокращения саркомеров в систолу и уменьшается степень их расслабления в диастолу на фоне повышенных потребностей клеток в АТФ. Это ведет к нарушению внутриклеточных сигнальных процессов и активации эмбриональных программ гипертрофического роста кардиомиоцитов. Кроме того, микроскопическая картина ГКМП характеризуется разволокнением мышечных волокон и фиброзом разной степени выраженности (феномен «disarray»). Дезорганизация кардиомиоцитов и замещение миокарда соединительной тканью ведут к снижению насосной функции сердца и предрасполагают к возникновению жизнеугрожающих тахиаритмий.
Макроскопическая картина ГКМП чаще всего характеризуется асимметричной гипертрофией межжелудочковой перегородки, которая сочетается с динамической обструкцией ВТЛЖ. Большую роль в развитии обструкции играет переднесистолическое движение передней створки митрального клапана (SAM-феномен), приводящее к резкому увеличению градиента давления в ВТЛЖ и к вторичной митральной регургитации [7]. Такое аномальное движение створки митрального клапана связывают с несколькими факторами: гипертрофией и смещением папиллярных мышц, удлинением створок и другими аномалия клапанного аппарата.
Длительное существование обструкции и гипертрофии межжелудочковой перегородки приводит к ухудшению релаксации миокарда, а также к увеличению ригидности стенок левого желудочка, что обуславливает развитие диастолической дисфункции, а в терминальной фазе заболевания – систолической дисфункции с прогрессированием симптомов сердечной недостаточности.
Клиническая картина
Клинические признаки ГКМП вариабельны – от бессимптомных до прогрессирующих форм, сопровождающихся тяжелой симптоматикой. Симптомы могут появляться или ухудшаться при воздействии факторов, которые увеличивают степень обструкции ВТЛЖ – при физических нагрузках, обезвоживании и применении некоторых препаратов, снижающих пред- или постнагрузку (диуретиков, гидралазина, ингибиторов АПФ, блокаторов рецепторов ангиотензина II, дигоксина).
Типичными проявлениями ГКМП являются [1, 5, 8]:
- одышка,
- боль в груди (атипичная или имеющая характер стенокардии),
- нарушение сердечного ритма (чаще всего – фибрилляция предсердий),
- головокружение,
- предобморочное состояние,
- обморок,
- внезапная сердечная смерть (может быть первым и единственным проявлением заболевания).
Диагностика
Физикальное обследование
При пальпации пациента с ГКМП может определяться усиленный, разлитой верхушечный толчок, смещенный влево и вниз. Нередко выявляется двухфазный пульс (pulsus bisferiens), характеризующийся двумя систолическими пиками.
Основным диагностическим признаком обструктивной ГКМП при аускультации является грубый систолический шум, который определяется на верхушке сердца и в четвертом межреберье слева. Данный шум низкочастотный, характеризуется нарастающе-убывающей интенсивностью (crescendo-decrescendo), выслушивается вдоль левого края грудины и усиливается под воздействием факторов, которые увеличивают внутрижелудочковый градиент давления: переход в вертикальное положение, физическая нагрузка, проба Вальсальвы, прием периферических вазодилататоров и др. Большинство пациентов с обструкцией ВТЛЖ также имеют аускультативные признаки митральной регургитации.
Генетическое тестирование
Проведение генетического тестирования рекомендуется всем пациентам с установленным диагнозом ГКМП для выявления мутации, которая стала причиной заболевания: в таком случае оно является инструментом диагностического поиска [1].
При выявлении патогенной мутации генетический скрининг проводится взрослым родственникам первой степени родства пациента: в этой ситуации генетическое тестирование носит предиктивный характер. Цель такого скрининга состоит в определении необходимости регулярной диспансеризации и прицельного клинического наблюдения родственников пациента с ГКМП.
Инструментальные методы исследования
Электрокардиография
Изменения на элетрокардиограмме (ЭКГ) выявляются у большинства больных, поэтому проведение стандартной ЭКГ в 12 отведениях рекомендуется при первичном обследовании пациентов с подозрением на ГКМП [1]. Кроме того, регистрация ЭКГ рекомендуется как компонент скрининг-алгоритма у родственников первой степени родства пациентов с ГКМП.
Несмотря на высокую чувствительность метода, изменения, определяемые при ГКМП, не являются специфичными:
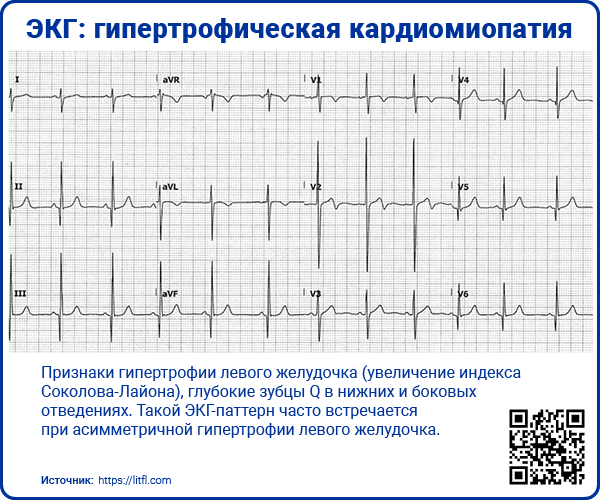
- Признаки гипертрофии левого желудочка (например, увеличение индекса Соколова-Лайона);
- Глубокие зубцы Q, особенно в нижних (II, III и aVF) и боковых (I, aVL, V4-6) отведениях (отражение деполяризации гипертрофированной ткани межжелудочковой перегородки);
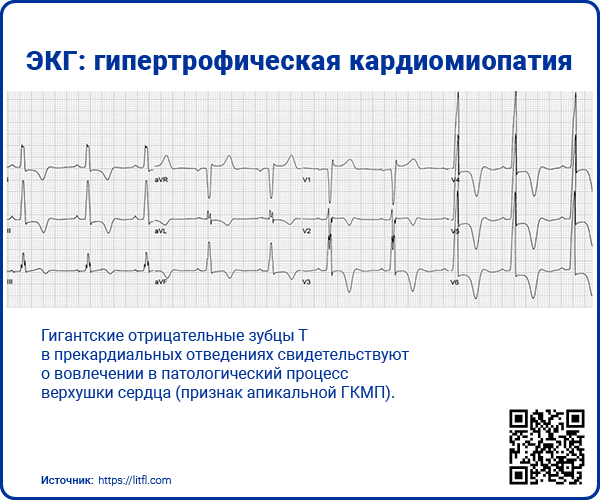
- Гигантские отрицательные зубцы T (>10 мм) в отведениях V2-4 (чаще всего регистрируются при апикальной или среднежелудочковой форме ГКМП).
Дополнительно могут определяться:
- Отклонение электрической оси сердца влево;
- Неспецифические изменения сегмента ST и зубца T (например, инверсия зубца T);
- Признаки гипертрофии левого предсердия (например, P-mitrale);
- Блокада левой ножки пучка Гиса (при выраженных фиброзных изменениях миокарда).
- Нарушения ритма (например, фибрилляция предсердий).
Холтеровское мониторирование ЭКГ рекомендуется пациентам с ГКМП для выявления нарушений ритма сердца и проводимости для стратификации риска внезапной сердечной смерти и отбора кандидатов для имплантации кардиовертера-дефибриллятора. Кроме того, показанием к длительному ЭКГ-мониторированию является появление у пациента жалоб на сердцебиение или головокружение.
Эхокардиография
Трансторакальная эхокардиография (ЭхоКГ) проводится всем пациентам с клиническим подозрением на ГКМП для верификации диагноза [1].
- Критерием диагноза у взрослых является увеличение толщины стенки левого желудочка в одном или более сегментах ≥15 мм, которое не объясняется исключительно перегрузкой давлением.
- У родственников пробанда критерий диагноза ГКМП – толщина стенки левого желудочка 13-14 мм и более.
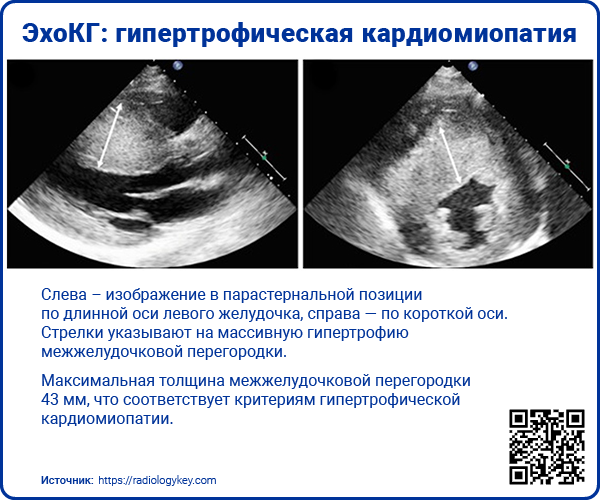
С помощью ЭхоКГ можно определить градиент давления в ВТЛЖ. Большинство европейских и американских исследователей критерием обструктивной ГКМП считают градиент ≥30 мм рт. ст. [5, 8].
Для определения латентной обструкции используются нагрузочные тесты (стресс-ЭхоКГ). С этой целью применяется лежачий велоэргометр, который позволяет получать ЭхоКГ-изображения на разных ступенях нагрузочной пробы. Использование тредмила и сидячего велоэргометра не позволяет регистрировать ЭхоКГ-показатели при проведении нагрузки, поэтому регистрация проводится немедленно после ее прекращения и в восстановительном периоде. При градиенте давления в ВТЛЖ <30 мм рт. ст. в покое и >30 мм рт. ст. при нагрузке диагностируют латентную обструкцию ВТЛЖ.
Важным ЭхоКГ-признаком ГКМП является наличие переднесистолического движения створки митрального клапана, однако SAM-феномен не относится к обязательным критериям для постановки диагноза ГКМП.
ЭхоКГ также позволяет:
- Оценить наличие или тяжесть митральной недостаточности;
- Измерить размеры левого предсердия;
- Оценить систолическую функцию левого желудочка.
МРТ сердца
МРТ сердца с контрастированием рекомендуется провести как минимум один раз после постановки диагноза ГКМП для уточнения данных ЭхоКГ (анатомии сердца, функции желудочков), выявления фиброза миокарда и исключения других заболеваний [1].
С помощью МРТ возможно идентифицировать:
- Области сегментарной гипертрофии левого желудочка, которые недостоверно визуализируются или недооцениваются по протяженности при ЭхоКГ.
- Структурные аномалии митрального клапана и папиллярных мышц.
- Структурные аномалии, предшествующие гипертрофии (например, апикальное смещение папиллярных мышц, миокардиальные крипты [9]).
МРТ с парамагнитным контрастным усилением используется для выявления и оценки распространенности фиброза миокарда: в сегментах миокарда с >15% фиброза выявляется феномен позднего накопления гадолиния, обусловленный задержкой вымывания контраста. Наличие распространенного фиброза является предиктором развития систолической дисфункции левого желудочка и относится к дополнительным факторам риска внезапной сердечной смерти.
МРТ сердца позволяет выявить ряд признаков, характерных для фенокопий ГКМП (амилоидоз сердца, болезнь Андерсона-Фабри и др.).
Катетеризация сердца
Катетеризация сердца проводится для оценки функции желудочков и давления заклинивания легочной артерии. Она рекомендована пациентам, которым планируется трансплантация сердца или механическая поддержка кровообращения, а также при несоответствии клинической картины и данных визуализации.
Стратификация риска внезапной сердечной смерти
5-летний риск внезапной сердечной смерти рекомендуется оценивать при первичном обследовании пациента с ГКМП и в дальнейшем – каждые 1-2 года или при изменении клинического статуса [1].
Существует две модели стратификации риска:
- Европейская модель (шкала HCM Risk-SCD) [10].
- Американская модель [5].

Лечение
Медикаментозное лечение
Лечение симптомной обструктивной ГКМП
Для уменьшения симптомов ГКМП в качестве первой линии терапии рекомендовано применение β-адреноблокаторов [1]:
При непереносимости или наличии противопоказаний к назначению β-адреноблокаторов препаратом второй линии является верапамил.
В том случае, если пациенту противопоказаны β-адреноблокаторы или верапамил, может быть назначен дилтиазем.
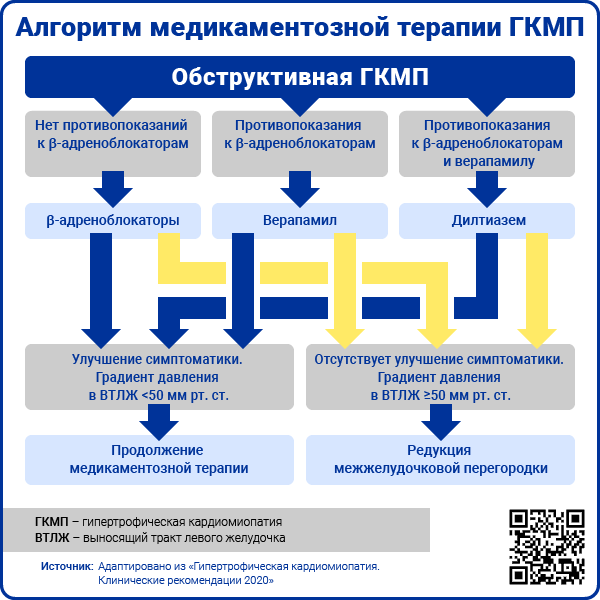
При неэффективности монотерапии β-адреноблокаторами и недигидропиридиновыми блокаторами кальциевых каналов возможно назначение комбинированной терапии с использованием дизопирамида [11]:
- β-адреноблокатор + дизопирамид,
- недигидропиридиновый блокатор кальциевых каналов + дизопирамид.
Пациентам с обструктивной ГКМП рекомендуется избегать назначения препаратов, приводящих к усилению обструкции ВТЛЖ [12]:
- сосудорасширяющие средства (дигидропиридиновые блокаторы кальциевых каналов, нитроглицерин, ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов ангиотензина II),
- диуретики в высоких дозах,
- дигоксин,
- спиронолактон.
Лечение хронической сердечной недостаточности
При фракции выброса левого желудочка ≥50% рекомендовано назначение монотерапии β-адреноблокаторами или недигидропиридиновыми блокаторами кальциевых каналов в качестве первой линии [1]. При объемной перегрузке возможно применение малых доз петлевых и тиазидных диуретиков.
При фракции выброса левого желудочка <50% пациентам назначают стандартную терапию ХСН со сниженной фракцией выброса, которая включает применение комбинации β-адреноблокаторов, ингибиторов АПФ, антагонистов альдостерона и диуретиков (при перегрузке объемом) [13].
Лечение стенокардии
При отсутствии обструктивной коронарной болезни сердца пациентам показано назначение β-адреноблокаторов, верапамила или дилтиазема в качестве первой линии терапии [1].
Для лечения стенокардии при ГКМП изучается эффективность ранолазина. Было показано, что регулярное применение препарата в течение 2 месяцев в дозе 500-1000 мг 2 раза в сутки приводит к облегчению стенокардии, симптомов сердечной недостаточности и улучшению качества жизни пациентов с ГКМП [14].
Лечение артериальной гипертензии
При необструктивной ГКМП лечение гипертонической болезни проводится в соответствии с текущими клиническими рекомендациями по лечению артериальной гипертензии у взрослых [15].
При обструктивной ГКМП антигипертензивная терапия включает в себя 3 этапа [1]:
- Прекращение приема периферических вазодилататоров.
- Назначение максимально переносимых доз β-адреноблокаторов, верапамила или комбинации обоих препаратов. Предпочтительно использовать пролонгированные и селективные β-адреноблокаторы (бисопролол, атенолол).
- Осторожное добавление низких доз гидрохлоротиазида с триамтереном под контролем градиента давления в ВТЛЖ.
Лечение фибрилляции предсердий
К задачам фармакотерапии ГКМП, осложненной фибрилляцией предсердий, относят [1]:
- Восстановление синусового ритма;
- Профилактика рецидивов аритмии;
- Профилактика тромбоэмболических осложнений.
При недавно возникшей фибрилляции предсердий (<48 часов от начала приступа) рекомендовано восстановление синусового ритма путем прямой электрической или фармакологической кардиоверсии с внутривенным введением амиодарона.
В том случае, если эпизод фибрилляции предсердий длится более 48 часов, рекомендуется воздержаться от незамедлительного восстановления синусового ритма. В этой ситуации возможно применение 2 стратегий:
- Ранняя кардиоверсия после чреспищеводной ЭхоКГ, не выявившей тромбы в полостях предсердий.
- Поздняя кардиоверсия (после 3 недель антикоагулянтной терапии) при невозможности проведения чреспищеводной ЭхоКГ или выявлении тромбов в полостях предсердий.
Для профилактики рецидивов аритмии возможно назначение следующих антиаритмических препаратов:
- амиодарон,
- соталол.
При ГКМП, осложненной фибрилляцией предсердий, назначают пожизненную антикоагулянтную терапию для профилактики тромбоэмболических осложнений. Возможно применение следующих препаратов:
- варфарин (целевое МНО 2.0-3.0),
- дабигатрана этексилат,
- ривароксабан,
- апиксабан.
В том случае, если пациент отказывается принимать эти препараты, возможно применение комбинации ацетилсалициловой кислотой с клопидогрелом [8].
Хирургическое и интервенционное лечение
Редукция межжелудочковой перегородки
Редукция межжелудочковой перегородки рекомендуется при ГКМП с градиентом давления в ВТЛЖ ≥50 мм рт. ст., симптомами ХСН III-IV функционального класса по NYHA, несмотря на максимальную переносимую терапию [1]. Для этого проводят септальную и расширенную миоэктомию, а также септальную алкогольную аблацию.
Септальная миоэктомия, или операция Морроу, заключается в трансаортальной резекции участка гипертрофированной межжелудочковой перегородки в области ВТЛЖ.
Помимо стандартной процедуры иссечения гипертрофированной межжелудочковой перегородки, нередко требуется коррекция сопутствующих аномалий митрального клапанного аппарата, которые вносят вклад в обструкцию ВТЛЖ. Это становится возможным при проведении расширенной миоэктомии, при которой область резекции расширяется в апикальном направлении к основанию папиллярных мышц. Иногда в англоязычной литературе данную процедуру называют RPR: resection – резекция гипертрофированного участка МЖП, plication – укорочение передней створки митрального клапана путем создания горизонтальной складки, release – освобождение или иссечение аномальных прикреплений гипертрофированных папиллярных мышц.
Процедура септальной алкогольной аблации выполняется при высоком хирургическом риске или наличии у пациента противопоказаний к открытому хирургическому вмешательству.
Техника операции заключается в транскатетерном введении 1-3 мл 95% спирта в перфорантную септальную ветвь, что в дальнейшем приводит к возникновению инфаркта гипертрофированного отдела межжелудочковой перегородки и уменьшению обструкции ВТЛЖ.
Было показано, что после проведения септальной алкогольной аблации наблюдается стойкое улучшение симптоматики в 76% случаев в течение первых 4 лет после операции, однако частота осложнений, возникающих при аблации, выше, чем при септальной миоэктомии [16]. Наиболее часто в послеоперационном периоде происходит нарушение внутрижелудочковой проводимости на уровне ножек пучка Гиса, что обуславливает необходимость постоянной электрокардиостимуляции при развитии полной атриовентрикулярной блокады.
Имплантация кардиовертера-дефибриллятора
Имплантация кардивертера-дефибриллятора проводится для профилактики внезапной сердечной смерти у пациентов с ГКМП.
Выделяют абсолютные и относительные показания к проведению этой процедуры.
Абсолютные показания:
- Остановка сердца в анамнезе;
- Документированный эпизод фибрилляции желудочков или желудочковой тахикардии.
Относительные показания:
- Предполагаемый 5-летний риск внезапной сердечной смерти ≥6% по европейской шкале [8].
- Наличие как минимум одного фактора риска из нижеперечисленных [5]:
- Семейный анамнез внезапной сердечной смерти из-за ГКМП;
- Максимальная толщина стенки левого желудочка ≥30 мм;
- 1 и более аритмогенных обмороков;
- Апикальная аневризма левого желудочка;
- Систолическая дисфункция левого желудочка (фракция выброса <50%).
Последние литературные данные показывают, что наличие распространенного фиброза, оцениваемого по позднему накоплению гадолиния при МРТ, является предиктором риска внезапной сердечной смерти при ГКМП [17]. Этот показатель не входит в европейскую модель стратификации риска, однако если у пациента риск внезапной сердечной смерти <6%, а при МРТ площадь фиброза >15% – это дополнительный аргумент в пользу имплантации кардиовертера-дефибриллятора.
Трансплантация сердца
Ортотопическая трансплантация сердца рекомендована пациентам с ГКМП, фракцией выброса левого желудочка <50% и симптомами ХСН III-IV функционального класса по NYHA или неустранимыми желудочковыми аритмиями, несмотря на проводимую терапию [1].
Сердечная ресинхронизирующая терапия
Пациентам с необструктивной ГКМП, фракцией выброса левого желудочка <50%, симптомами ХСН II-IV функционального класса по NYHA и блокадой левой ножки пучка Гиса с длительностью QRS >120 мс возможно проведение сердечной ресинхронизирующей терапии для устранения симптомов болезни [1].
Список литературы
- Габрусенко С. А. и др. Гипертрофическая кардиомиопатия. Клинические рекомендации 2020 //Российский кардиологический журнал. – 2021. – №. 5. – С. 269-334.
- Amano Y. et al. MRI classification of asymmetric septal hypertrophic cardiomyopathy and its relation to the presence of risk factors //The international journal of cardiovascular imaging. – 2012. – Т. 28. – С. 2019-2025.
- Geske J. B., Ommen S. R., Gersh B. J. Hypertrophic cardiomyopathy: clinical update //JACC: heart failure. – 2018. – Т. 6. – №. 5. – С. 364-375.
- Дземешкевич С. Л. и др. Анатомические и морфологические признаки диффузно-генерализованной формы гипертрофической кардиомиопатии //Российский кардиологический журнал. – 2015. – №. 5 (121). – С. 58-63.
- Ommen S. R. et al. 2020 AHA/ACC guideline for the diagnosis and treatment of patients with hypertrophic cardiomyopathy: executive summary: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines //Journal of the American College of Cardiology. – 2020. – Т. 76. – №. 25. – С. 3022-3055.
- Marian A. J., Braunwald E. Hypertrophic cardiomyopathy: genetics, pathogenesis, clinical manifestations, diagnosis, and therapy //Circulation research. – 2017. – Т. 121. – №. 7. – С. 749-770.
- Varma P. K., Neema P. K. Hypertrophic cardiomyopathy: part 1-introduction, pathology and pathophysiology //Annals of cardiac anaesthesia. – 2014. – Т. 17. – №. 2. – С. 118-124.
- Elliott P. M. et al. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy //Kardiologia Polska (Polish Heart Journal). – 2014. – Т. 72. – №. 11. – С. 1054-1126.
- Brouwer W. P. et al. Multiple myocardial crypts on modified long-axis view are a specific finding in pre-hypertrophic HCM mutation carriers //European Heart Journal–Cardiovascular Imaging. – 2012. – Т. 13. – №. 4. – С. 292-297.
- O'Mahony C. et al. A novel clinical risk prediction model for sudden cardiac death in hypertrophic cardiomyopathy (HCM risk-SCD) //European heart journal. – 2014. – Т. 35. – №. 30. – С. 2010-2020.
- Verlinden N. J., Coons J. C. Disopyramide for hypertrophic cardiomyopathy: a pragmatic reappraisal of an old drug //Pharmacotherapy: The Journal of Human Pharmacology and Drug Therapy. – 2015. – Т. 35. – №. 12. – С. 1164-1172.
- Roberts R., Sigwart U. Current concepts of the pathogenesis and treatment of hypertrophic cardiomyopathy //Circulation. – 2005. – Т. 112. – №. 2. – С. 293-296.
- Терещенко С. Н. и др. Хроническая сердечная недостаточность. Клинические рекомендации 2020 //Российский кардиологический журнал. – 2020. – №. 11. – С. 311-374.
- Gentry J. L. et al. Ranolazine for treatment of angina or dyspnea in hypertrophic cardiomyopathy patients (RHYME) //Journal of the American College of Cardiology. – 2016. – Т. 68. – №. 16. – С. 1815-1817.
- Клинические рекомендации. Артериальная гипертензия у взрослых. – 2022.
- Maron B. J. Commentary and re-appraisal: surgical septal myectomy vs. alcohol ablation: after a decade of controversy and mismatch between clinical practice and guidelines //Progress in cardiovascular diseases. – 2012. – Т. 54. – №. 6. – С. 523-528.
- Desai M., Mentias A. Risk stratification in hypertrophic cardiomyopathy //Aging (Albany NY). – 2019. – Т. 11. – №. 6. – С. 1617.
Описание проверено экспертом
Статьи по теме Кардиология
- Инфекционный эндокардит
- Хроническая сердечная недостаточность
- Миокардит
- Синдром слабости синусового узла
- Атриовентрикулярная блокада
- Внутрижелудочковая блокада
- Митральный стеноз
- Внезапная остановка сердца
- Острый инфаркт миокарда
- Желудочковая тахикардия
- Тромбоэмболия легочной артерии
- Акушерская тромбоэмболия
- Ожирение
Болезни в статье:
- I46.1 Внезапная сердечная смерть, так описанная
- I50.0 Застойная сердечная недостаточность
- I48 Фибрилляция и трепетание предсердий
- I20 Стенокардия [грудная жаба]
- I25.3 Аневризма сердца
- E85 Амилоидоз
- E75.2 Другие сфинголипидозы
- E74.0 Болезни накопления гликогена
- G11.1 Ранняя мозжечковая атаксия
- Q87.1 Синдромы врожденных аномалий, проявляющихся преимущественно карликовостью
- Q87.8 Другие уточненные синдромы врожденных аномалий, не классифицированные в других рубриках
- I10 Эссенциальная (первичная) гипертензия
- I44.6 Другие и неуточненные блокады пучка
- I44.2 Предсердно-желудочковая блокада полная
- I46.0 Остановка сердца с успешным восстановлением сердечной деятельности
- I49.0 Фибрилляция и трепетание желудочков
- I47.2 Желудочковая тахикардия
- I44.7 Блокада левой ножки пучка неуточненная
Фармгруппы в статье:
- Диуретики
- Ингибиторы АПФ
- Антагонисты рецепторов ангиотензина II (AT1-подтип)
- Бета-адреноблокаторы
- Блокаторы кальциевых каналов
- Антикоагулянты
Оцените статью:
- Кардиомиопатия гипертрофическая обструктивная
- Гипертрофическая кардиомиопатия
- Гипертрофическая обструктивная кардиомиопатия
- Гипертрофия миокарда с обструкцией
- Ассиметричная гипертрофия межжелудочковой перегородки
- Облитерирущая рестриктивная кардиомиопатия
- Обструктивная ГКМП
Гипертрофическая кардиомиопатия: генетическая ловушка для сердца
От первых описаний до современных методов лечения: как учёные научились бороться с ГКМП?
Опубликовано на сайте: 18.03.25 | Обновлено на сайте: 18.03.25
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).
гипертрофическая обструктивная кардиомиопатия
обструкция выносящего тракта левого желудочка
субаортальный стеноз
гипертрофическая кардиомиопатия
гипертрофическая обструктивная кардиомиопатия, гипертрофическая обструктивная кардиомиопатия (ГОКМП), у пациентов с гипертрофической обструктивной кардиомиопатиеи, гипертрофической обструктивной кардиомиопатии, гипертрофической обструктивной кардиомиопатии (ГОКМП), гипертрофическая обструктивная кардиомиопатия [ГОКМП], гипертрофическую обструктивную кардиомиопатию, гипертрофической обструктивной кардиомиопатией, идиопатическая гипертрофическая обструктивная кардиомиопатия (ГОКМП), обструктивной кардиомиопатией, гипертрофическая обструктивная миокардиопатия, гипертрофической обструктивной кардиомиопатией (ГОКМП), обструкция выносящего тракта левого желудочка, нарушение оттока крови из левого желудочка, гемодинамически значимая обструкция выносящего тракта левого желудочка (включая аортальный стеноз), гемодинамически значимая обструкция выносящего тракта ЛЖ (включая тяжелый аортальный стеноз), гемодинамически значимая обструкция выносящего тракта левого желудочка (включая тяжелый аортальный стеноз), Патологические состояния, приводящие к обструкции выносящего тракта левого желудочка: выраженный стеноз устья аорты, Патологические состояния, приводящие к обструкции выносящего тракта левого желудочка: гипертрофическая обструктивная кардиомиопатия, гемодинамически значимое сужение выходного отдела левого желудочка, механическая обструкция, препятствующая заполнению или выбросу крови из желудочков, обструкция выходного отдела левого желудочка, обструктивные заболевания выводного отдела левого желудочка сердца, обструкция выходного тракта левого желудочка, состояния, затрудняющие отток крови из левого желудочка, Гемодинамически значимая обструкция выносящего тракта левого желудочка, гемодинамический значимый стеноз выносящего тракта сердца, Обструкция выносящего тракта левого желудочка сердца, гемодинамически значимое нарушение оттока крови из левого желудочка, затруднении выброса крови из левого желудочка, гемодинамически значимое нарушение оттока крови из ЛЖ, Динамический стеноз выносящего тракта сердца, Гемодинамически значимая обструкция выходного тракта левого желудочка, обструкция выходящего тракта левого желудочка, Обструкция выводного тракта левого желудочка, идиопатический субаортальный стеноз, идиопатический гипертрофический субаортальный стеноз, идиопатический гипертрофический субаортальный стеноз (ИГСС), субаортальный стеноз, тяжелый субаортальный стеноз, гипертрофический обструктивный субаортальный стеноз, идиопатическом подклапанном аортальном стенозе, идиопатическом гипертрофическом субаортальном стенозе, гипертрофический субаортальный стеноз, идиопатическом субаортальном стенозе, Заболевания, сопровождающиеся обструкцией выносящего тракта левого желудочка (гипертрофическая кардиомиопатия), гипертрофической кардиомиопатии, гипертрофическая кардиомиопатия, гипертрофическая кардиомиопатия (ГОКМП), гипертрофической кардиомиопатией,