C43.4 Злокачественная меланома волосистой части головы и шеи, МКБ-10
Отредактировано: 19.09.2023
д.м.н., проф. Демидов Л.В., к.м.н. Харкевич Г.Ю., к.м.н. Маркина И.Г.
ГУ РОНЦ им. Н.Н. Блохина РАМН
д.м.н., проф. Молочков В.А., к.м.н. Снарская Е.С., д.м.н. Лезвинская Е.М., д.м.н. Молочков А.В., д.м.н., проф. Казанцева И.А.
РМАПО Министерства здравоохранения и социального развития РФ
Предрак кожи. Болезнь Боуэна. Эритроплазия Кейра. Плоскоклеточный рак кожи. Базалиома. Метатипический рак кожи. Кожная и внекожная формы меланомы. Злокачественные лимфомы кожи. Саркома Капоши
Заболеваемость злокачественными опухолями, поражающими основание черепа, составляет около 0,4 на 100 тыс. населения в год. Такие опухоли, особенно при поражении ТМО и распространении в полость черепа, традиционно считались радикально неоперабельными и часто вообще инкурабельными. Современное развитие нейрохирургии, онкологии и пластической хирургии привело к появлению новых, достаточно эффективных методов лечения таких больных.
Опухоль возникает чаще из эпителия придаточных пазух носа (рак), встречаются саркомы, нейроэпителиома и злокачественная опухоль оболочек периферического нерва, плазмоцитома и злокачественная гистиоцитома.
Существует множество частных классификаций, основанных на месте исходного роста новообразования. Универсальна и все чаще применяемая — классификация ТNМ.
Подход к лечению злокачественных опухолей — комплексный, имеющий существенные отличия от такового при доброкачественных опухолях основания черепа. Комбинированный метод лечения, применение которого обязательно при злокачественных опухолях, включает в себя хирургические, лучевые и химиотерапевтические методы. Выбор оптимальной тактики, включая последовательность применения указанных методов, определяется гистологической природой и распространенностью опухоли.
Клинические проявления злокачественных опухолей, вторично распространяющихся в полость черепа, на ранних этапах неспецифичны, заболевание вначале обычно протекает под маской хронических воспалительных процессов. К специалисту (чаще — онкологу, реже — нейрохирургу) больные обращаются в поздней стадии заболевания и в большинстве случаев на момент постановки диагноза опухоли относятся к ТЗ–4, NО–2, МО–1.
Распространение опухоли в полость черепа происходит как при разрушении кости, так и по ходу черепных нервов. Соответственно у больных обычно имеет место болевой синдром (особенно интенсивный при вовлечении в процесс ветвей тройничного нерва), могут выявляться признаки нарушения функции черепных нервов, при значительном распространении опухоли в полость черепа присоединяются общемозговые и очаговые симптомы.
Диагноз уточняется при МРТ, обычно с контрастным усилением (что позволяет успешнее дифференцировать опухоль от мягких тканей шеи). Костные изменения лучше выявляются при КТ, причем трехмерная КТ-реконструкция облегчает планирование метода пластики дефекта после резекции пораженной кости.
Помимо этих, традиционно используемых в нейрохирургии методов, для оценки состояния лимфатических узлов шеи больным целесообразно производить УЗИ шеи, радионуклидную лимфографию, а также рентгено(томо)графию или КТ органов грудной клетки, ультразвуковое или КТ исследование органов брюшной полости.
Обязательная (за очень редкими исключениями) составляющая диагностического комплекса — предоперационная биопсия опухоли. Она может выполняться открытым, пункционным или эндоскопическим способами, выбор определяется локализацией опухоли.
После уточнения диагноза перечисленными методами на консилиуме с участием онкологов, нейрохирургов, пластических хирургов, радиологов, химиотерапевтов и при необходимости представителей других специальностей определяется тактика лечения больного.
Общий план лечения больных с операбельными опухолями следующий.
При раке — последовательно — предоперационная химиотерапия, канцеростатическая доза лучевой терапии, удаление опухоли, лучевая терапия, повторные курсы химиотерапии.
При саркомах — хирургическое лечение с послеоперационным курсом лучевой терапии, при хондросаркомах и хордомах альтернативой становится радиохирургия.
При опухолях лимфоретикулярного ряда (плазмоцитома, злокачественная гистиоцитомы) — лучевая терапия в сочетании с химиотерапией при необходимости, для лимфом — химиотерапия, дополняемая при недостаточном эффекте лучевой терапией.
При злокачественной опухоли оболочек периферического нерва — хирургическое лечение, послеоперационный полный курс лучевой терапии, поддерживающие курсы химиотерапии в позднем послеоперационном периоде.
Хирургическое вмешательство может быть радикальным или паллиативным.
Радикальное вмешательство показано при Т1–3 Nx М0 стадии процесса, в остальных ситуациях при показаниях возможно выполнение паллиативного вмешательства. При индексе Карновского 30 и ниже хирургическое лечение не показано.
Следует отметить, что местные гнойные процессы, обусловленные как нарушением дренажа околоносовых пазух, так и распадом и нагноением опухоли, не являются противопоказанием к проведению радикальной или паллиативной операции.
У больных с III стадией опухолевого процесса хирургическое вмешательство, заключающееся в максимально возможном удалении опухоли, приводит к образованию обширных дефектов черепа и мягких тканей, которые необходимо закрывать с применением различных методов пластики. Области хирургической доступности (возможности радикального удаления опухоли основания черепа) схематично представлены на рисунке 1. Медиальные отделы основания черепа (зона Г) не могут быть включены в блок, расположенные там опухоли относятся к Т4 стадии.
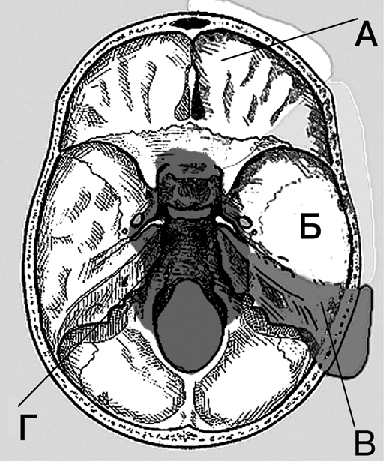
Рисунок 1. Зоны локализации опухолей, доступные для радикального хирургического лечения (блок-резекции):
Основной принцип краниофациальной резекции — формирование и удаление блока тканей, внутри которого находится опухоль. При этом, в зависимости от локализации процесса, объем включенной в блок непораженной опухолью ткани может быть различным. Ограничений при формировании блока носоглотки, верхнечелюстной и решетчатой пазух практически нет. При выделении блока в области передней черепной ямки в него можно включить ТМО, обонятельные нервы и даже инфильтрированную опухолью базальную кору лобной доли. Однако при распространении опухоли в направлении средней черепной ямки после удаления основного блока производится дополнительное иссечение пораженной ТМО в области зрительного канала, верхней и нижней глазничных щелей, передних отделов кавернозного синуса, т.е. часть опухоли приходится удалять не единым блоком в пределах здоровых тканей, а фрагментированием.
Сложности возникают и в случаях поражения одной из глазниц с вовлечением решетчатой пазухи, включая медиальную стенку противоположной глазницы. При этом в блок может быть включена пораженная глазница, решетчатая пазуха, а из другой, “здоровой”, глазницы в блок можно включить прилежащие отделы надкостницы, жировой клетчатки. При обширном поражении обеих глазниц применяются паллиативные методы лечения.
Таким образом, при краниофациальных блок-резекциях нет четких рекомендаций, какой слой прилежащих к опухоли тканей должен быть включен в блок. В передней черепной ямке это может быть 3–5 мм, в носоглотке и верхнечелюстной пазухе — 2–3 см. При прорастании опухолью кожа включается в блок. Если кожа мобильна и между ней и опухолью имеется слой непораженных тканей, она в блок не включается. После удаления блока целесообразно для повышения радикальности произвести дополнительное иссечение сомнительных тканей, которые могут быть инфильтрированы распространяющейся опухолью.
После удаления опухоли дефект ТМО закрывают лоскутом надкостницы или свободным лоскутом жировой клетчатки из передней брюшной стенки с фиксацией швами или фибрин-тромбиновым клеем. Этот лоскут дополняется вторым, надкостнично-фасциальным, лоскутом на ножке. При обширных дефектах применяются более сложные методы пластики (лоскутом большого сальника, кожно-мышечным лоскутом прямой мышцы живота, лоскутом большой грудной мышцы, кожно-мышечным лоскутом передней зубчатой мышцы и фрагментами ребер) (рис. 2). При необходимости последующего протезирования глазного яблока пластика дефекта мягких тканей осуществляется с учетом этого обстоятельства.
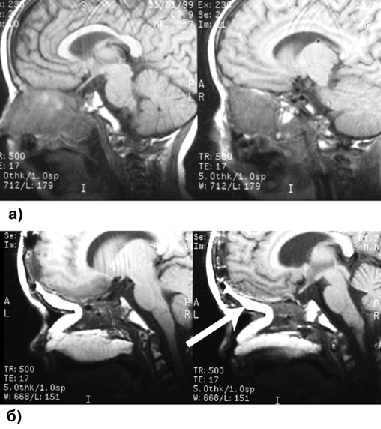
Рисунок 2. МРТ до (а) и после (б) операции больного с рабдомиосаркомой решетчатой пазухи, носоглотки, правой половины полости носа, правой гайморовой пазухи. Стрелкой показан трансплантат прямой мышцы живота
Люмбальный дренаж целесообразно устанавливать перед операцией и удалять на 6–10 сутки. Питание больных осуществляется через устанавливаемый перед операцией назогастральный зонд, который удаляется на 7–15 сутки.
При значительной распространенности процесса на шее целесообразно после блок-резекции формирование трахеостомы и гастростомы.
При распространении опухоли на латеральные отделы основания черепа в блок включаются структуры, формирующие подвисочную ямку, суставной и венечный отростки нижней челюсти, наружные отделы пирамиды височной кости, верхнечелюстная пазуха, глазница, основание передней черепной ямки, формирующее крышу глазницы. Дефекты закрываются по тем же принципам, что и при передних блок-резекциях.
При распространении опухоли на височную кость также возможны радикальные вмешательства. Боковая резекция подразумевает частичную мастоидэктомию и иссечение хрящевого и костного отделов наружного слухового канала с включением структур барабанной полости в зависимости от глубины распространения опухоли. Полная резекция производится при опухолях, захватывающих среднее ухо и/или систему воздухоносных ячеек сосцевидного отростка. Внутренняя граница резекции при этом проходит на уровне лабиринта и проксимальных отделов внутреннего слухового прохода. При пирамидной резекции, которая применяется при распространении опухоли на большую часть пирамиды височной кости, внутренняя граница резекции проходит латеральнее канала внутренней сонной артерии. Наиболее обширной является петрокливальная блок-резекция, при которой в блок удаляемых тканей включается верхушка пирамиды височной кости со вскрытием канала внутренней сонной артерии, с реконструкцией последней или без таковой.
При тщательном отборе больных, после включающего блок-резекцию комбинированного лечения 5-летняя общая выживаемость превышает 50%, безрецидивная — 20%.
Паллиативные операции. Показаниями к проведению паллиативных операций является необходимость уменьшения объема опухоли (в связи с выраженным изменением внутричерепных объемных соотношений) и создания условий для проведения курсов лучевой и химиотерапии. Рецидивирующие кровотечения из опухоли, обильное кровоснабжение стромы новообразования служат показаниями к эмболизации афферентных сосудов опухоли либо как основное паллиативное вмешательство, либо как подготовка к радикальному хирургическому лечению. Выбор хирургического доступа при паллиативной операции обусловливается локализацией и распространением основного процесса, а технические приемы удаления опухоли в целом идентичны таковым при радикальной операции.
Литература
Janecka I.P. et al. Skull Base Surgery/Anatomy, Biology and Technology. Philadelphia-New-York: Lippincott-Raven, 1996.
Robertson J.T. et al. Cranial Base Surgery.— London: Churchill Livingston, 2000.
Meyers I.N. et al. eds. Cancer of the head and neck 2nd edition.— NY: Churchill Livingstone, 1989.
Описание проверено экспертом
Оцените статью:
Могут ли татуировки снижать риск меланомы?
Новое исследование показало: у людей с несколькими татуировками риск развития меланомы оказался ниже, чем у тех, кто их не имеет.
Опубликовано на сайте: 21.10.25 | Обновлено на сайте: 20.10.25
Ультрафиолетовые лампы и рак кожи: стоит ли бояться маникюра
Новые исследования показывают, что УФ-лампы для гель-лака не столь опасны, как принято считать, если соблюдать простые правила защиты.
Опубликовано на сайте: 10.11.25 | Обновлено на сайте: 01.11.25
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).






